题目内容
【题目】有一瓶标签被腐蚀的稀硫酸,小江为了测定溶液中溶质的质量分数,用NaOH固体和水配制40g 10%的NaOH溶液于烧杯中,然后往烧杯中滴加稀硫酸,反应过程中溶液的pH与滴入稀硫酸的质量关系下图所示:
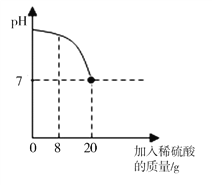
请计算:(已知:2NaOH+ H2SO4= Na2SO4+2H2O)
(1)配制40g 10%的NaOH溶液,需要水的质量为 g;
(2)该稀硫酸中H2SO4质量分数(写出计算过程)。
【答案】(1)36g;(2)24.5%
【解析】(1)配制40g 10%的NaOH溶液,需要水的质量为∶40g-40g×10%=36g;
(2)解∶设该稀硫酸中H2SO4质量分数为x,
2NaOH+ H2SO4= Na2SO4+2H2O
80 98
40g×10% 20g×x
![]() =
=![]() ,x=24.5%.
,x=24.5%.
答∶(1)配制40g 10%的NaOH溶液,需要水的质量为36g;(2)该稀硫酸中H2SO4质量分数是24.5%。
点睛∶本题主要考查溶液的组成以及根据化学方程式进行计算。

练习册系列答案
相关题目
【题目】下表是氯化钠和碳酸钠在不同温度时的溶解度,根据此表回答:
温度/℃ | 10 | 20 | 30 | 40 | |
溶解度/g | 氯化钠 | 35.8 | 36.0 | 36.3 | 36.6 |
碳酸钠 | 12.2 | 21.8 | 39.7 | 53.2 | |
(1)40℃时,氯化钠的溶解度为________g。
(2)碳酸钠溶液中混有少量的氯化钠,可通过________结晶方法提纯。
(3)在20℃时,在100g水中加入25 g碳酸钠,充分搅拌后得到的是_____(填“饱和”或“不饱和”)溶液,将上述溶液升温到30℃,所得溶液的溶质质量分数为________。