题目内容
过氧化钠(Na2O2)与水发生反应,生成对应的碱和氧气,化学方程式为:2Na2O2+2H2O=4NaOH+O2↑.现将一定质量的过氧化钠投入400g水中,充分反应,产生32克氧气.试计算:
(1)参加反应的过氧化钠的质量是多少?
(2)反应后所得溶液的质量是多少?
解:设参加反应的过氧化钠的质量为x
2Na2O2+2H2O=4NaOH+O2↑
156 32
x 32g

x=156 g
反应后所得溶液的质量是:156g+400g-32g=524g
答:(1)参加反应的过氧化钠的质量156 g;(2)反应后所得溶液的质量524g.
分析:(1)根据质量守恒定律可以根据氧气的质量求出参加反应的过氧化钠的质量进行解答;
(2)根据反应的化学方程式可以知道反应后的溶液为氢氧化钠溶液,可以根据氧气的质量结合化学方程式求算出氢氧化钠的质量,进而求算出氢氧化钠溶液的质量.
点评:要想解答好这类题目,首先,要理解和熟记根据化学反应方程式的计算步骤和格式,以及与之相关的知识等.然后,根据所给的问题情景,结合所学的相关知识和技能,细致地分析题意并细心地探究、推理后,按照题目要求进行认真地解答即可.
2Na2O2+2H2O=4NaOH+O2↑
156 32
x 32g

x=156 g
反应后所得溶液的质量是:156g+400g-32g=524g
答:(1)参加反应的过氧化钠的质量156 g;(2)反应后所得溶液的质量524g.
分析:(1)根据质量守恒定律可以根据氧气的质量求出参加反应的过氧化钠的质量进行解答;
(2)根据反应的化学方程式可以知道反应后的溶液为氢氧化钠溶液,可以根据氧气的质量结合化学方程式求算出氢氧化钠的质量,进而求算出氢氧化钠溶液的质量.
点评:要想解答好这类题目,首先,要理解和熟记根据化学反应方程式的计算步骤和格式,以及与之相关的知识等.然后,根据所给的问题情景,结合所学的相关知识和技能,细致地分析题意并细心地探究、推理后,按照题目要求进行认真地解答即可.

练习册系列答案
相关题目
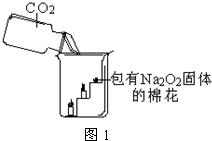


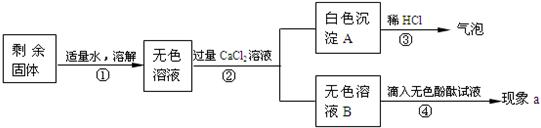
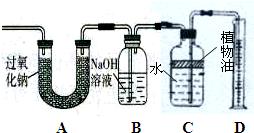 23、呼吸面具和潜水艇中可用过氧化钠(Na2O2)作为供氧剂.下面是兴趣小组同学围绕过氧化钠进行的一系列探究,请你参与到其中.
23、呼吸面具和潜水艇中可用过氧化钠(Na2O2)作为供氧剂.下面是兴趣小组同学围绕过氧化钠进行的一系列探究,请你参与到其中.