题目内容
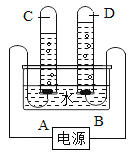
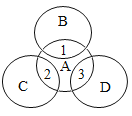
【题目】A、B、C、D分别是铁、盐酸、碳酸钠溶液、氢氧化钠溶液中的一种,其应关系如图所示,图中两圆相交部分1、2、3表示两种物质间反应的主要现象,其中1无明显现象。请思考下列问题:
(1)A与D反应的产物之一可作灭火剂,则2的现象是__________________。
(2)A与C反应的化学方程式:____________________,其基本反应类为__________。A与D反应的化学方程式:_________________________。
(3)要验证A与D反应得到的气体产物,可将其通入_____________中,反应的化学方程式是_____。
【答案】有气泡产生,溶液由无色变为浅绿色 Fe+2HCl═FeCl2+H2↑ 置换反应 Na2CO3+2HCl═2NaCl+H2O+CO2↑ 澄清石灰水 Ca(OH)2+CO2═CaCO3↓+H2O
【解析】
所给物质中只有盐酸能与其它物质发生反应,铁与盐酸反应生成氯化亚铁和氢气,碳酸钠与盐酸反应生成氯化钠、水、二氧化碳,盐酸与氢氧化钠反应生成氯化钠和水,由图示可知只有A能与其余三种物质都反应,所以A是盐酸,由于二氧化碳既不能燃烧也不支持燃烧,且密度比空气大,所以可以用来灭火,A与D反应的产物之一可作灭火剂,即产生二氧化碳,所以D是碳酸钠,由其中1无明显现象,可知B是氢氧化钠,因为氢氧化钠与盐酸反应生成氯化钠和水,没有现象.
(1)铁与盐酸反应生成氯化亚铁和氢气,亚铁离子溶液是浅绿色,所以反应现象是:有气泡产生,溶液由无色变为浅绿色;
(2)A与C反应的反应物是铁和盐酸,生成物是氯化亚铁和氢气,用观察法配平,氢气后面标上上升符号,即Fe+2HCl═FeCl2+H2↑;反应物中有一种是单质,有一种是化合物,生成物中有一种是单质,有一种是化合物,所以反应类型是置换反应;A与D反应的反应物是碳酸钠和盐酸,生成物是氯化钠、水和二氧化碳,用观察法配平,二氧化碳后面标上上升符号,即Na2CO3+2HCl═2NaCl+H2O+CO2↑;
(3)A与D反应得到的气体产物是二氧化碳,二氧化碳的检验方法是:将气体通入澄清石灰水中,石灰水变浑浊,说明该气体是二氧化碳,反应物是二氧化碳和氢氧化钙,生成物是碳酸钙和水,碳酸钙后面标上沉淀符号,即Ca(OH)2+CO2═CaCO3↓+H2O.
故答案为:(1)有气泡产生,溶液由无色变为浅绿色;(2)Fe+2HCl═FeCl2+H2↑;置换反应;Na2CO3+2HCl═2NaCl+H2O+CO2↑;(3)澄清石灰水;Ca(OH)2+CO2═CaCO3↓+H2O.

 备战中考寒假系列答案
备战中考寒假系列答案【题目】除去下列物质中的杂质(括号内为杂质),所选用试剂及操作均正确的一组是( )
选项 | 待提纯的物质 | 选用的试剂 | 操作方法 |
A |
| 稀 | 加适量的稀硫酸、蒸发结晶 |
B | NaCl( |
| 加入过量 |
C |
|
稀HCl | ①加过量 ②再向沉淀中滴加适量稀盐酸 |
D | CaO( | 稀HCl | 加入足量的稀盐酸,过滤、洗涤、干燥 |
A.AB.BC.CD.D