题目内容
【题目】根据如图装置,回答下列有关问题. 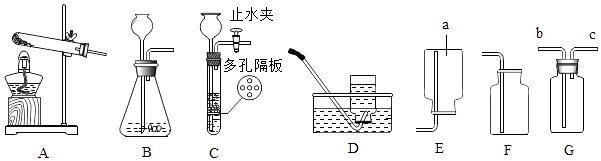
(1)装置图中仪器a的名称为;
(2)实验室用KMnO4制取O2应选用的一套实验装置为(填装置编号)该反应的化学方程式为;
(3)实验室用石灰石和稀盐酸制取二氧化碳的化学方程式为;
(4)常温下,可用固体硫化亚铁(FeS)和稀硫酸反应制取硫化氢(H2S)气体,可选择的发生装置是(填装置编号).若用充满水的G装置收集H2 , 气体从(填“b”或“c”)处导管进入.
(5)某同学向过氧化氢溶液中加入二氧化锰制取氧气,相关数据如下:
反应前物质的质量/g | 充分反应后物质的质量/g | |
过氧化氢溶液 | 二氧化锰 | 固体与液体混合物质量 |
68.0 | 0.1 | 66.5 |
请计算:
①该同学制得氧气的质量为多少?
②该同学所用过氧化氢溶液的溶质质量分数为多少?
【答案】
(1)集气瓶
(2)AD或AF;2KMnO4 ![]() K2MnO4+MnO2+O2↑
K2MnO4+MnO2+O2↑
(3)CaCO3+2HCl=CaCl2+H2O+CO2↑
(4)B或C;c
(5)解:根据质量守恒定律,该同学制得氧气的质量=68.0g+0.1g﹣66.5g=1.6g;
设该同学所用过氧化氢溶液的溶质质量分数为x,
2H2O2 |
| 2H2O+ | O2↑ |
68 | 32 | ||
68.0gx | 1.6g |
![]()
x=0.5%;
答:该同学制得氧气的质量为1.6g;该同学所用过氧化氢溶液的溶质质量分数为0.5%;
【解析】解:(1)集气瓶是收集气体的仪器,所以答案是:集气瓶;(2)如果用高锰酸钾制氧气就需要加热,高锰酸钾受热分解生成锰酸钾和二氧化锰和氧气,要注意配平;氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集;所以答案是:AD或AF;2KMnO4 ![]() K2MnO4+MnO2+O2↑;(3)实验室制取CO2 , 是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热;所以答案是:CaCO3+2HCl=CaCl2+H2O+CO2↑;(4)常温下,可用固体硫化亚铁(FeS)和稀硫酸反应制取硫化氢(H2S)气体,因此不需要加热;若用充满水的G装置收集H2 , 气体从短管进入,因为氢气的密度比比水小;所以答案是:B或C;c;
K2MnO4+MnO2+O2↑;(3)实验室制取CO2 , 是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热;所以答案是:CaCO3+2HCl=CaCl2+H2O+CO2↑;(4)常温下,可用固体硫化亚铁(FeS)和稀硫酸反应制取硫化氢(H2S)气体,因此不需要加热;若用充满水的G装置收集H2 , 气体从短管进入,因为氢气的密度比比水小;所以答案是:B或C;c;
【考点精析】解答此题的关键在于理解书写化学方程式、文字表达式、电离方程式的相关知识,掌握注意:a、配平 b、条件 c、箭号,以及对根据化学反应方程式的计算的理解,了解各物质间质量比=系数×相对分子质量之比.