��Ŀ����
����Ŀ��ij������Ʒ�к��������Ȼ������ʡ���ȡ����Ʒ22.8g�����뵽ʢ��һ������ϡ������ձ��У�̼������ϡ����ǡ����ȫ��Ӧ��������ȫ�ݳ����õ�������NaCl��Һ����Ӧ�����в���ձ��ڻ�����������m���뷴Ӧʱ�䣨t����ϵ��ͼ��ʾ���Իش�
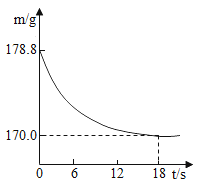
��1������CO2������_____��
��2��22.8g��Ʒ���Ȼ��Ƶ�����Ϊ_____��
��3������������Һ�����ʵ���������_________����д�������̣���������ȷ��0.1%��
���𰸡�8.8g 1.6g 14.7%
��������
��1����ͼ��������غ㶨�ɿ�֪�����ɶ�����̼������Ϊ��178.8g��170.0g��8.8g��
��2����̼���Ƶ�����Ϊx�������Ȼ��Ƶ�����Ϊy��
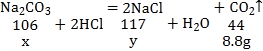
![]() ��ã�x��21.2g��y��23.4g��
��ã�x��21.2g��y��23.4g��
22.8g��Ʒ���Ȼ��Ƶ�����Ϊ��22.8g��21.2g��1.6g
��3����ȫ��Ӧ�������Ȼ�����Һ��������������![]() 14.7%
14.7%
�ʴ�Ϊ����1��8.8��
��2��22.8g��Ʒ���Ȼ��Ƶ�����Ϊ1.6g��
��3��������Һ�����ʵ���������Ϊ14.7%��

��ϰ��ϵ�д�
�����Ŀ