题目内容
【题目】某热电厂用脱硫得到的石膏(CaSO4·2H2O)生产K2SO4肥料的流程如图:
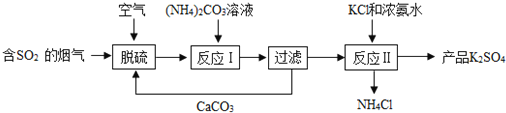
(1)脱硫过程中可用_____喷淋烟气来吸收SO2.
(2)石膏与饱和(NH4)2CO3溶液相混合,发生反应Ⅰ时需不断搅拌,其目的是____
(3)上述流程中可循环使用的物质是______(填写化学式);
(4)用饱和K2SO4溶液洗涤反应Ⅱ所得晶体,不用水洗涤的原因是_____.
【答案】水或碱溶液 使反应物充分接触,提高原料利用率 CaCO3 防止硫酸钾溶于水
【解析】
(1)二氧化硫能和水反应生成亚硫酸,能和碱溶液反应生成盐和水;
(2)反应物接触越充分,反应速率越快,反应也越彻底;
(3)根据图中的工艺流程可以判断可循环使用的物质;
(4)硫酸钾易溶于水,不溶于饱和硫酸钾溶液.
(1)二氧化硫能和水反应生成亚硫酸,能和碱溶液反应生成盐和水,因此脱硫过程中可用水或碱溶液喷淋烟气来吸收SO2.
故填:水或碱溶液.
(2)石膏与饱和(NH4)2CO3溶液相混合,发生反应Ⅰ时不断搅拌,其目的是使反应物充分接触,提高原料利用率.
故填:使反应物充分接触,提高原料利用率.
(3)硫酸钙和碳酸铵反应生成硫酸铵和碳酸钙,过滤后碳酸钙被重新加入到脱硫中去,反应又生成硫酸钙,因此上述流程中可循环使用的物质是CaCO3.
故填:CaCO3.
(4)用饱和K2SO4溶液洗涤反应Ⅱ所得晶体,不用水洗涤的原因是防止硫酸钾溶于水.
故填:防止硫酸钾溶于水.

 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案【题目】实验室有一瓶长期暴露在空气中的氢氧化钠固体样品,观察发现,样品表面有白色的粉末。某兴趣小组的同学对该样品的成分及含量进行了探究。
(提出问题1)该样品中含有哪些物质?
(提出猜想)通过分析,提出如下猜想:
猜想Ⅰ:已完全变质,该样品中只含![]() ;
;
猜想Ⅱ:部分变质,该样品中含有NaOH和Na2CO3。
则变质反应的化学方程式为_____。
(查阅资料)①碱性的Na2CO3溶液可以与中型的CaCl2溶液发生复分解反应;
②![]() 在饱和的碳酸氢钠溶液中几乎不溶解。
在饱和的碳酸氢钠溶液中几乎不溶解。
(实验探究1)为确定该样品的成分,小明设计了如下实验方案,请你一起完成下列实验。
实验操作 | 实验现象 | 实验结论 |
(1)取少量样品溶于水,加入 ____ | 白色沉淀产生 | 该反应的化学方程式:___ |
(2)将上述反应后的混合液过滤,取滤液加入____ | ______ | 证明猜想Ⅱ成立 |
(提出问题2)如何测量该部分变质样品中碳酸钠的质量分数?
(实验探究2)小红同学设计如图装置(铁架台略去),实验在27℃,101KPa下进行,步骤如下:①按图连接好装置;②用托盘天平准确称取该样品2g,放入A中试管内,向B中集气瓶中倒入饱和碳酸氢钠溶液至瓶颈处;③向分液漏斗中加入稀硫酸,打开活塞,让稀硫酸滴入试管中至过量,关闭活塞.反应结束后,量筒中收集到饱和碳酸氢氧化钠溶液220mL。请回答下列问题:
(1)在实验步骤①和②之间,还缺少一实验步骤,该实验步骤是 _________ ;
(2)B中集气瓶盛装的饱和碳酸氢钠溶液不能用水代替,其理由是 ________ ;
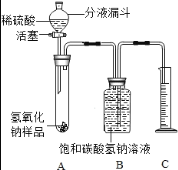
(3)试管中原有的空气对实验结果是否有明显影响? ___ (填“有”或“没有”);
(4)变质氢氧化钠样品中碳酸钠的质量分数为 __________。(在27℃,101KPa时二氧化碳的密度为1.8g/L)(计算结果精确至1%)
(提出问题3)怎样提纯该样品得到纯净的氢氧化钠固体?
(实验探究3)为得到纯净的氢氧化钠固体,小亮设计了如图的实验流程。
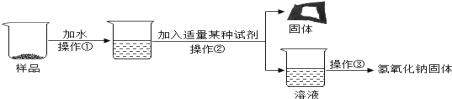
请回答下列问题:
(1)为了使样品充分溶解,操作①中还要用到的玻璃仪器是_________ ;操作③中加热到____________时停止加热。
(2)该实验中发生反应的化学方程式为 ____________ ;
(3)最终所得氢氧化钠固体质量 ________ 变质后样品中氢氧化钠的质量(填“小于”、“等于”或“大于”)。