题目内容
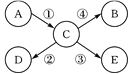
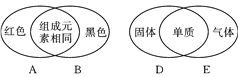
【题目】构成物质的粒子之间的关系如图所示:
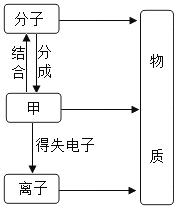
(1)甲是_____.
(2)在水,汞,氯化钠三物质中,由离子组成的物质是_____,保持水化学性质的最小粒子是_____.
(3)电解水试验可证明水的组成,其反应的化学方程式为_____,在该实验中,加入少量硫酸钠可增强水的导电性(在通电前后硫酸钠的质量和性质不变),现有0.2g硫酸钠溶解在99.8g水中并通电,当溶液中硫酸钠的质量分数为0.25%时,有_____g水被电解.
【答案】原子 氯化钠 水分子 2H2O![]() 2H2↑+O2↑ 20
2H2↑+O2↑ 20
【解析】
(1)构成物质的微粒有分子、原子、离子,分子是由原子构成的,原子通过得失电子形成离子,由离子构成物质.故答案为:原子;
(2)构成物质的微粒有分子、原子和离子,金属汞是由汞原子构成的,水是由水分子构成的,氯化钠是由钠离子和氯离子构成的.保持水的化学性质的最小粒子是水分子;
(3)水通电分解生成氢气和氧气,反应的化学方程式为2H2O![]() 2H2↑+O2↑;
2H2↑+O2↑;
硫酸钠在通电前后质量和性质不变,所以电解水完毕后溶液质量为:![]() =80g,溶液质量减少了:0.2克+99.8克﹣80克=20克.
=80g,溶液质量减少了:0.2克+99.8克﹣80克=20克.
答案:(1)原子;(2)氯化钠;水分子;(3)2H2O![]() 2H2↑+O2↑;20.
2H2↑+O2↑;20.

练习册系列答案
相关题目