题目内容
能源和环境是当今人类面临的两大问题.目前,化石燃料是人类生产、生活的主要能源.随着全球能源使用量的增长及不科学使用,化石燃料等不可再生能源将日益枯竭,并对环境产生严重影响.这就迫切要求人们开发氢能、太阳能等新能源.(1)氢能来源广泛,是高能清洁能源.氢气除了可直接燃烧获得热量外,还可设计成燃料电池.目前使用氢能还面临着氢气的制取和氢气的储存两个问题.如图为模拟氢、氧燃料电池的实验装置.X、Y均为纱布袋做成的容器,装有活性炭,并与内部的石墨棒紧密接触,导线与石墨连接(石墨和活性炭都能导电).把X、Y浸在水中,并在水中加一些稀硫酸,以增强水的导电能力.当电键K与b接通,发生反应的化学方程式为 .通电一段时间内没有看到气泡逸出,是因为活性炭具有 性,从而解决了气体储存的问题.此时将电键K与a接通,灯泡发光,说明能量发生了如下转化:氢能→ 能→光能和热能.
(2)一些常用燃料燃烧时的热值如下表:
| 燃料 | 天然气(以CH4计) | 液化气(以C4H10计) | 原煤(以C计) |
| 热值(kJ/g) | 约56 | 约50 | 约33 |
②化石燃料燃烧放出的CO2是一种温室气体,大量向空气中排放CO2将对气候产生负面影响.试通过计算说明,当上表中天然气和液化气充分燃烧获得相等的热量时,哪一种燃料放出的CO2较少?

【答案】分析:(1)根据方程式的书写、活性炭的结构特点、能量的转化关系考虑;(2)①根据原煤燃烧后产生污染考虑;②利用放出相同的热量进行计算.
解答:解:(1)电解水的反应物是水,生成物时氢气和氧气,用观察法配平即可,反应条件是电解写在等号上边,氢气和氧气后面标上上升符号,所以方程式为2H2O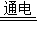 2H2↑+O2↑;由于活性炭具有疏松多孔的结构所以具有吸附性;由于灯泡发光需要有电,所以氢能转化为电能;
2H2↑+O2↑;由于活性炭具有疏松多孔的结构所以具有吸附性;由于灯泡发光需要有电,所以氢能转化为电能;
(2)①原煤含有硫等有害元素,燃烧产生SO2污染空气 燃烧产生大量粉尘污染空气热值低等,
②设都放出QkJ的热量,m(CH4) 和m(C4H10)分别为:
m(CH4)=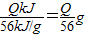 ;m(C4H10)=
;m(C4H10)=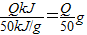
设这些质量的甲烷完全燃烧产生二氧化碳质量为m(CO2)甲烷
则:
CH4+2O2 CO2+2H2O
CO2+2H2O
16 44
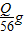 m(CO2)甲烷
m(CO2)甲烷
 解得m(CO2)甲烷=0.049Qg
解得m(CO2)甲烷=0.049Qg
设这些质量的液化气燃烧产生二氧化碳质量为m(CO2)液化气
则:
2C4H10+13O2 8CO2+20H2O
8CO2+20H2O
2×58 8×44
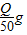 m(CO2)液化气
m(CO2)液化气
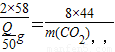 解得m(CO2)液化气=0.061Qg
解得m(CO2)液化气=0.061Qg
m(CO2)甲烷<m(CO2)液化气
故答案为:(1)2H2O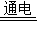 2H2↑+O2↑ 吸附 电能(2)①原煤含有硫等有害元素,燃烧产生SO2污染空气 燃烧产生大量粉尘污染空气 热值低等,②天然气.
2H2↑+O2↑ 吸附 电能(2)①原煤含有硫等有害元素,燃烧产生SO2污染空气 燃烧产生大量粉尘污染空气 热值低等,②天然气.
点评:解答本题关键是方程式书写方法,热量的计算方法,通过计算进行比较.
解答:解:(1)电解水的反应物是水,生成物时氢气和氧气,用观察法配平即可,反应条件是电解写在等号上边,氢气和氧气后面标上上升符号,所以方程式为2H2O
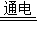 2H2↑+O2↑;由于活性炭具有疏松多孔的结构所以具有吸附性;由于灯泡发光需要有电,所以氢能转化为电能;
2H2↑+O2↑;由于活性炭具有疏松多孔的结构所以具有吸附性;由于灯泡发光需要有电,所以氢能转化为电能;(2)①原煤含有硫等有害元素,燃烧产生SO2污染空气 燃烧产生大量粉尘污染空气热值低等,
②设都放出QkJ的热量,m(CH4) 和m(C4H10)分别为:
m(CH4)=
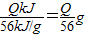 ;m(C4H10)=
;m(C4H10)=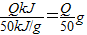
设这些质量的甲烷完全燃烧产生二氧化碳质量为m(CO2)甲烷
则:
CH4+2O2
 CO2+2H2O
CO2+2H2O16 44
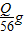 m(CO2)甲烷
m(CO2)甲烷 解得m(CO2)甲烷=0.049Qg
解得m(CO2)甲烷=0.049Qg设这些质量的液化气燃烧产生二氧化碳质量为m(CO2)液化气
则:
2C4H10+13O2
 8CO2+20H2O
8CO2+20H2O2×58 8×44
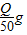 m(CO2)液化气
m(CO2)液化气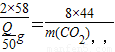 解得m(CO2)液化气=0.061Qg
解得m(CO2)液化气=0.061Qg m(CO2)甲烷<m(CO2)液化气
故答案为:(1)2H2O
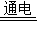 2H2↑+O2↑ 吸附 电能(2)①原煤含有硫等有害元素,燃烧产生SO2污染空气 燃烧产生大量粉尘污染空气 热值低等,②天然气.
2H2↑+O2↑ 吸附 电能(2)①原煤含有硫等有害元素,燃烧产生SO2污染空气 燃烧产生大量粉尘污染空气 热值低等,②天然气.点评:解答本题关键是方程式书写方法,热量的计算方法,通过计算进行比较.

练习册系列答案
相关题目
 (2006?镇江)能源和环境是当今人类面临的两大问题.目前,化石燃料是人类生产、生活的主要能源.随着全球能源使用量的增长及不科学使用,化石燃料等不可再生能源将日益枯竭,并对环境产生严重影响.这就迫切要求人们开发氢能、太阳能等新能源.
(2006?镇江)能源和环境是当今人类面临的两大问题.目前,化石燃料是人类生产、生活的主要能源.随着全球能源使用量的增长及不科学使用,化石燃料等不可再生能源将日益枯竭,并对环境产生严重影响.这就迫切要求人们开发氢能、太阳能等新能源. 能源和环境是当今人类面临的两大问题.目前,化石燃料是人类生产、生活的主要能源.我国天然气的储量丰富,合理开发和使用是国人面临的共同课题.
能源和环境是当今人类面临的两大问题.目前,化石燃料是人类生产、生活的主要能源.我国天然气的储量丰富,合理开发和使用是国人面临的共同课题.