题目内容
(6分)某食盐样品中含有少量沙土、氯化钙和氯化镁.以下是除去食盐样品中沙土、氯化钙和氯化镁的实验流程:
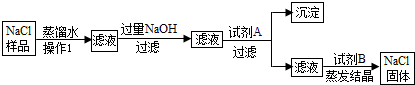
根据流程图回答:
(1)操作Ⅰ的名称是 ,加入的试剂A是 ,沉淀是
;
(2)写出NaOH与杂质反应的化学方程式 ;
(3)加入试剂B的目的是 ;
(4)蒸发结晶时用到玻璃棒的作用是 。

根据流程图回答:
(1)操作Ⅰ的名称是 ,加入的试剂A是 ,沉淀是
;
(2)写出NaOH与杂质反应的化学方程式 ;
(3)加入试剂B的目的是 ;
(4)蒸发结晶时用到玻璃棒的作用是 。
(1)过滤 Na2CO3 =CaCO3
(2)2NaOH + MgCl2 = Mg(OH)2↓ + 2NaCl
(3)除去NaOH和Na2CO3
(4)防止局部温度过高,造成液滴飞溅
(2)2NaOH + MgCl2 = Mg(OH)2↓ + 2NaCl
(3)除去NaOH和Na2CO3
(4)防止局部温度过高,造成液滴飞溅
试题分析:(1)操作Ⅰ是将不溶性固体也液体分离,所以名称为:过滤,在滤液中加入过量的NaOH溶液是除去杂质氯化镁,故接下来加入的试剂A,是为了除去氯化钙,所以加入的试剂A应是Na2CO3溶液,发生反应:CaCl2+Na2CO3==CaCO3↓+2NaCl,所以沉淀是:=CaCO3
(2)根据上面的分析,NaOH与杂质反应的化学方程式:2NaOH + MgCl2 = Mg(OH)2↓ + 2NaCl
(3)由于前面所加试剂都是过量,所以试剂B是将前面所加过量的NaOH和Na2CO3除去
(4)蒸发结晶时用到玻璃棒的作用是:防止局部温度过高,造成液滴飞溅

练习册系列答案
相关题目