题目内容
学完酸碱盐知识后,小美对妈妈焙制糕点用的小苏打很感兴趣,她把小苏打带到实验室与小刚一起进行探究。
(1)小美取少量小苏打溶于水,滴加酚酞试液后,溶液变红,说明小苏打的水溶液显 性;
(2)小刚在烧杯内放入少量小苏打,向其中滴加稀盐酸,立即有 产生,说明小苏打能与酸反应。在医疗上可以用小苏打治疗 ;
(3)小美想:糕点非常松软,是不是小苏打受热分解产生了CO2气体呢?于是她用下图装置对小苏打进行加热,一段时间后,导管口的确有气泡冒出,澄清石灰水变浑浊,同时试管口有水珠生成。
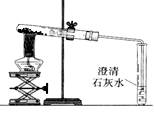
当导管口不再有气泡产生时,试管内仍有白色固体,她猜测剩余固体可能是:①NaOH;②Na2CO3;③NaCl。小刚认为猜想
一定不正确,理由是 。小刚从试管内取少量白色固体溶于水,滴加酚酞,溶液变红,他判断该固体为NaOH,小美认为他的实验设计不合理,因为
(4)小美和小刚继续探究固体成分,设计了如下实验:
通过实验证明小苏打受热会分解,反应的化学方程式为: 。通过本次探究学习,小美对小苏打的性质有了全面的认识,她给妈妈提出保存小苏打的建议有: (答出一点即可)。
(1)小美取少量小苏打溶于水,滴加酚酞试液后,溶液变红,说明小苏打的水溶液显 性;
(2)小刚在烧杯内放入少量小苏打,向其中滴加稀盐酸,立即有 产生,说明小苏打能与酸反应。在医疗上可以用小苏打治疗 ;
(3)小美想:糕点非常松软,是不是小苏打受热分解产生了CO2气体呢?于是她用下图装置对小苏打进行加热,一段时间后,导管口的确有气泡冒出,澄清石灰水变浑浊,同时试管口有水珠生成。

当导管口不再有气泡产生时,试管内仍有白色固体,她猜测剩余固体可能是:①NaOH;②Na2CO3;③NaCl。小刚认为猜想
一定不正确,理由是 。小刚从试管内取少量白色固体溶于水,滴加酚酞,溶液变红,他判断该固体为NaOH,小美认为他的实验设计不合理,因为
(4)小美和小刚继续探究固体成分,设计了如下实验:
| 操作步骤 | 实验现象 | 结论 |
| 取少量白色固体于试管中,加水溶解,向其中滴加 溶液 | 产生白色沉淀 | 试管内剩余的固体为Na2CO3 |
碱性;气泡,胃酸过多;③,碳酸氢钠中不含氯元素;碳酸钠溶液也呈碱性;氯化钙溶液;
NaHCO3="==" Na2CO3+H2O+CO2↑;低温保存。
NaHCO3="==" Na2CO3+H2O+CO2↑;低温保存。
试题分析:(1)碱性溶液能使酚酞变成红色;
(2)小苏打是碳酸氢钠,能与盐酸反应生成二氧化碳气体,医疗上常用于治疗胃酸过多;
(3)根据质量守恒定律化学反应前后元素的种类不变,由于碳酸氢钠中不含氯元素,故不可能生成氯化钠;由于碳酸钠溶液也呈碱性,也能使无数酚酞变红,故不能通过加指示剂来确定;
(4)根据结论,试管内剩余的固体为Na2CO3,碳酸钠能与氯化钙反应生成碳酸钙白色沉淀;由实验探究可知碳酸氢钠分解生成了二氧化碳和碳酸钠,利用质量守恒定律,另一张生成物是水;碳酸氢钠高温易分解,故要在低温干燥处保存。

练习册系列答案
 优生乐园系列答案
优生乐园系列答案
相关题目