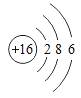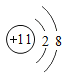题目内容
【题目】利用氯化钠配制溶液,进行如下实验:
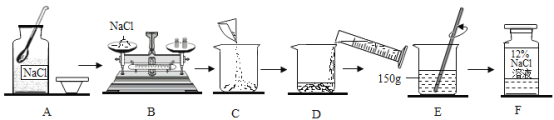
请根据示意图回答:
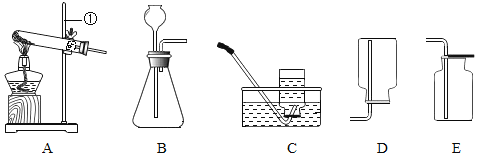
(1)上述操作中,有错误的是_____(填字母)。
(2)通过计算可知,托盘天平左盘中固体氯化钠的质量应为_____![]() ;在称量氯化钠的过程中,同学发现托盘天平的指针偏向右盘,应_____(填字母);
;在称量氯化钠的过程中,同学发现托盘天平的指针偏向右盘,应_____(填字母);
A增加适量氯化钠固体 B减少适量氯化钠固体 C调节平衡螺母
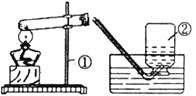
(3)操作![]() 中,玻璃棒的作用是_____。
中,玻璃棒的作用是_____。
(4)下列情况可能会造成所配制溶液中溶质的质量分数偏小的是_____(填字母)。
A得到的![]() 未完全干燥
未完全干燥
B用量筒量取水时,仰视读数
C配好的溶液装瓶中,烧杯内有溶液残留
【答案】A 18 A 搅拌,加速溶解 ABC
【解析】
(1)A、取用固体药品氯化钠,取用时,应将瓶塞倒放在桌面上,防止药品被污染。A操作错误;
B、称量氯化钠,应当遵循“左物右码”。B操作正确;
C、将称量好的氯化钠转移到烧杯中。C操作正确;
D、将量筒的水倒入烧杯中进行溶解。D操作正确;
E、用玻璃棒不断地搅拌,使其充分溶解。E操作正确;
F、装入到细口瓶中,并贴上标签。F操作正确。
故答案为:A;
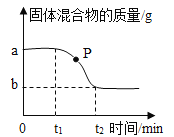
(2)由图E可知,溶液的总质量为150g,由图F可知,溶质的质量分数为12%。故可以通过溶液乘溶质的质量分数计算出溶质的质量,即:150g×12%=18g;计算后进行称量,应当是先调节托盘天平的平衡螺母后,将18g砝码放在右盘,随后进行称量。若在称量过程中,发现天平指针偏向右盘,说明药品仍然不足18g,所以此时应该添加氯化钠固体药品。故答案为:18、A;
(3)操作E是搅拌,目的是为了加速溶解过程。故答案为:搅拌,加速溶解;
(4)A、得到的氯化钠未完全干燥,则称量出来的18g是“氯化钠+水”的质量,氯化钠不足18g,会导致溶质质量分数偏小;
B、用量筒量取水时,仰视读数,则量取的水的体积会偏多。溶质的质量分数=![]() ,量取水的体积偏多,则溶剂偏多,则质量分数偏小;
,量取水的体积偏多,则溶剂偏多,则质量分数偏小;
C、烧杯中溶液有残留,则溶质和溶剂同时减小,则分数值也减小。故答案为:ABC。

 习题精选系列答案
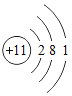
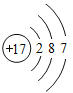
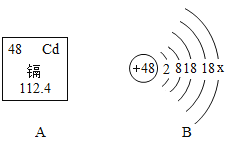
习题精选系列答案【题目】下图是常见的粒子结构示意图,请根据粒子结构示意图回答下列问题:
粒 子 结 构 示意图 |
|
|
|
|
编 号 | A | B | C | D |
(1)上述微粒示意图中表示阳离子的是_____(填编号)。
(2)由同一种元素B形成的单质是_____(填化学式)。
(3)上述微粒中属于同一种元素的是_____(填编号)。
(4)元素C在化学反应中表现出的最高化合价是_____价,C元素最高价与氧元素形成氧化物的化学式是_____。