题目内容
将锌粉放入含有Mg(NO3)2、Cu(NO3)2、AgNO3三种溶质的混合溶液中,充分反应后,过滤,得不溶物和滤液;向滤液中滴加稀盐酸,无明显现象.由此可知析出的不溶物中一定含有( )
| A、Cu、Ag | B、Ag |
| C、Mg、Cu、Ag | D、Cu |
考点:金属的化学性质
专题:金属与金属材料
分析:根据金属活动性由强到弱的关系(Mg>Zn>Cu>Ag),锌可置换硝酸银中的银、锌可置换硝酸铜中的铜,生成的铜还可以置换硝酸银中的银,而锌与Mg(NO3)2不反应.充分反应后向滤液中滴加稀盐酸无明显现象,说明了溶液中没有硝酸银,根据以上反应及现象,分析反应的发生情况,推断所得固体.
解答:解:
由题意可知,向Mg(NO3)2、AgNO3和Cu(NO3)2混合溶液中加入一定量的锌粉,发生的反应有锌可置换硝酸银中的银、锌可置换硝酸铜中的铜,生成的铜还可以置换硝酸银中的银,而锌与Mg(NO3)2不反应.充分反应后再向滤液中滴加稀盐酸无明显现象,说明了溶液中没有硝酸银.根据锌的量不一定,则析出的不溶物中铜可能含有,而银一定含有,镁一定不存在.
故选:B.
由题意可知,向Mg(NO3)2、AgNO3和Cu(NO3)2混合溶液中加入一定量的锌粉,发生的反应有锌可置换硝酸银中的银、锌可置换硝酸铜中的铜,生成的铜还可以置换硝酸银中的银,而锌与Mg(NO3)2不反应.充分反应后再向滤液中滴加稀盐酸无明显现象,说明了溶液中没有硝酸银.根据锌的量不一定,则析出的不溶物中铜可能含有,而银一定含有,镁一定不存在.
故选:B.
点评:主要考查了对金属活动性顺序的应用,根据金属活动性顺序来判断反应的发生,培养学生分析问题、应用知识的能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列反应既是氧化,又是化合的是( )
A、铜+氧气
| ||
B、酒精+氧气
| ||
| C、碳酸→水+二氧化碳 | ||
D、碳+氧化铜
|
若用“ ”表示X原子,用“
”表示X原子,用“ ”表示Y原子,下图为它们反应的示意图,下列说法不正确的( )
”表示Y原子,下图为它们反应的示意图,下列说法不正确的( )
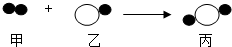
 ”表示X原子,用“
”表示X原子,用“ ”表示Y原子,下图为它们反应的示意图,下列说法不正确的( )
”表示Y原子,下图为它们反应的示意图,下列说法不正确的( )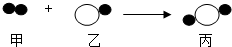
| A、乙和丙的元素种类相同 |
| B、甲和丙中同种元素化合价相等 |
| C、该反应属于化合反应 |
| D、甲、乙、丙的化学计量数之比为1:2:2 |
食用下列食品,不会对人体健康造成危害的是( )
| A、用工业食盐腌制的泡菜 |
| B、用甲醛溶液浸泡的海产品 |
| C、霉变的花生、大米 |
| D、牛奶经发酵后得到的酸奶 |
学习化学时会遇到很多“相等”,下列有关“相等”的说法中错误的是( )
| A、原子中核内质子总数和核外电子总数一定相等 |
| B、中和反应时参加反应的酸和碱的质量一定相等 |
| C、溶液稀释前后溶质的质量一定相等 |
| D、物质发生化学变化前后,元素的种类一定相等 |
下列符号中,表示一个原子,又表示一种元素,还表示一种物质的是( )
| A、H2 |
| B、Ag |
| C、2H2 |
| D、2H |
黑火药是我国四大发明之一,黑火药的爆炸可用2KNO3+3C+S═K2S+N2+3X表示,则X的化学式为( )
| A、CO |
| B、SO2 |
| C、NO |
| D、CO2 |
 通过化学学习,我们形成了一些化学基本观念.
通过化学学习,我们形成了一些化学基本观念. ”代表碳原子,“
”代表碳原子,“ ”代表氧原子).
”代表氧原子).