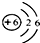题目内容
碳是形成化合物种类最多的元素,含碳物质是中学化学研究的重要内容。
(1)“低碳生活”倡导低能量、低消耗,主要是为了减少 (填化学式)的排放量。
(2)右图为元素周期表中的一格,下列说法不正确的是 (填标号)。

 A.碳元素属于非金属元素
A.碳元素属于非金属元素
 B.碳原子核内质子数为6
B.碳原子核内质子数为6
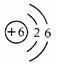
C.碳元素的原子结构示意图为
D.碳的相对原子质量为12.01
(3)甲、乙、丙、丁是初中化学常见的化合物,甲和乙中含有碳元素,丙能做干燥剂。它们之间有如右图所示的转化关系(部分物质和反应条件已略去)。则甲的化学式为 ;丙转化为丁的化学力。程式为 。

(4)右边是某趣味实验装置图。挤压胶头滴管后,可观察到气球胀大的现象。请分析其原因,并写出化学方程式。

(5)利用下图装置可做CO还原Fe2O3,的实验,并检验该反应生成的气体产物。已知由A装置制取的CO气体中混有少量的CO2。

①CO与Fe2O3反应的化学方程式为 。
②气体通过装置的顺序是A→ (装置不能重复使用)。
③从环保角度考虑,对以上装置的改进措施是 。
(6)称取12.5g石灰石(主要成分是CaCO3,杂质不参加反应)放人烧杯中,向其中加入50g稀盐酸,二者恰好完全反应。反应结束后称量烧杯中剩余物质的总质量为58.1g(不包括烧杯的质量,且气体的溶解忽略不计)。试计算石灰石中杂质的质量分数。
(1)CO2 (1分) (2)C (1分)
(3)CaCO3 (1分) CaO+H2O=Ca(OH) 2 (1分)
(4)CO2被浓NaOH溶液吸收,锥形瓶内的气压成小,外界大气压大于锥形瓶内的气压,使气球胀大。 (1分) 2NaOH+CO2=Na2CO3+H2O (1分)
高温
(5)①Fe2O3+3C0=====2Fe+3CO2 (1分) ②C→D→B (1分)
③将尾气点燃或进行收集等。 (1分)
(6)解:生成CO2的质量为: 12.5 g+50 g-58.1g=4.4g (1分)
设石灰石中CaCO3的质量为x。
CaCO3+2HCl=CaCI2+CO2↑+H2O (1分)
100 44
x 4.4g
![]() x=10g
x=10g
石灰石中杂质的质量分数为:
![]() ×100%=20%(1分)
×100%=20%(1分)
答:石灰石中杂质的质量分数为20%。

 碳是形成化合物种类最多的元素,含碳物质是中学化学研究的重要内容.
碳是形成化合物种类最多的元素,含碳物质是中学化学研究的重要内容. 碳是形成化合物种类最多的元素,含碳物质是中学化学研究的重要内容.
碳是形成化合物种类最多的元素,含碳物质是中学化学研究的重要内容.
 碳是形成化合物种类最多的元素,含碳物质是中学化学研究的重要内容.
碳是形成化合物种类最多的元素,含碳物质是中学化学研究的重要内容. D.碳的相对原子质量为12.01
D.碳的相对原子质量为12.01
 碳是形成化合物种类最多的元素,含碳物质是中学化学研究的重要内容.
碳是形成化合物种类最多的元素,含碳物质是中学化学研究的重要内容.