题目内容
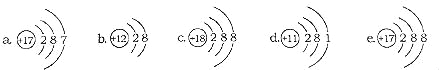
【题目】图一是镓原子的有关信息图,图二是某反应的微观模拟图。请回答
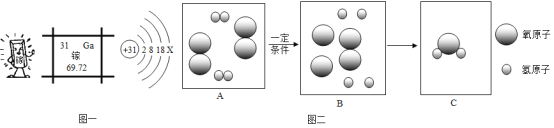
(1)镓是一种奇妙的金属,放在手心马上熔化,说明镓的_____________。
(2)在元素周期表中,镓元素排第________周期;3个镓离子可表示为_____________。
(3)请在图二C中将需要补充的相关粒子补画完整__________。
【答案】熔点低 四 3Ga3+ 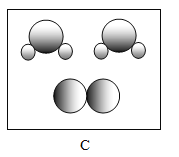
【解析】
(1)镓放在手心马上熔化,说明人体的体温就能使镓熔化,也就是镓熔点低;
故填:熔点低。
(2)在镓原子的结构示意图中,核外有4个电子层,在元素周期表中,位于第四周期,镓原子的最外层有3个电子,在化学反应中,易失去3个电子,带3个单位的正电荷,离子表示为Ga3+,三个镓离子表示为3Ga3+;
故填:四;3Ga3+。
(3)在图二A中,有2个氢分子、2个氧分子;B中2个氢分子分裂为4个氢原子,1个氧分子分裂为2个氧原子,还有1个氧分子;在C中,2个氢原子与1个氧原子构成1个水分子;在C中,有2个水分子,1个未反应的氧分子;
故填: 。
。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
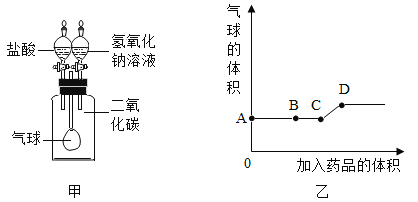
小学生10分钟应用题系列答案【题目】化学兴趣小组为验证质量守恒定律,做了镁条在空气中然烧的实验(如图1)。
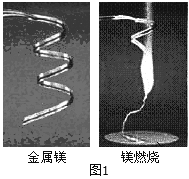
(1)根据镁燃烧发出耀眼的白光这一特点,在军事上用于制造_____;
(2)同学们通过称量发现:即使不考虑参加反应的氧气的质量,在石棉网上收集到产物的质量也小于烧掉镁条的质量,看似该反应不遵循质量守恒定律。请你分析出现这种结果的原因可能是:_____;
(3)小红按图2装置进行实验,结果符合质量守恒定律,同时还发现产物中有少量黄色固体。决定探究黄色固体为何物。
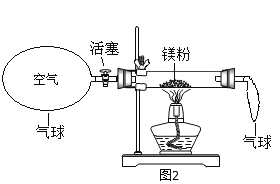
(提出问题)黄色固体是什么?
(查阅资料)得到如下信息①氧化镁为白色固体;②镁能与氮气剧烈反应生成黄色的氮化镁(Mg3N2)固体:③氮化镁可与水剧烈反应产生氨气;④氨气有刺激性气味,能使湿润的红色石蕊试纸变蓝。
(做出猜想)黄色固体可能是Mg3N2;
(实验探究)请设计实验,验证猜想:
实验操作 | 实验现象 | 结论 |
_____ | _____ | 黄色固体是Mg3N2 |
(反思交流)
①写出镁条燃烧生成氮化镁的化学方程式为_____;
②空气中N2的含量远大于O2的含量,可是镁条在空气中燃烧产物MgO却远多于Mg3N2,合理的解释是_____。
③氢气也可以在氯气中能够燃烧,反应方程式为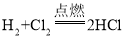 。结合以上事实,请你谈一谈对燃烧的新认识_____。
。结合以上事实,请你谈一谈对燃烧的新认识_____。