题目内容
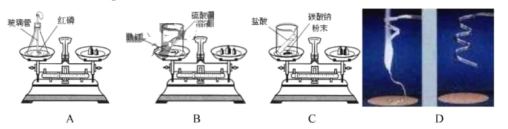
【题目】(1)相同质量的镁、铝、锌分别与相同质量20%的盐酸充分反应,产生氢气质量(直接用各金属表示,例如:Mg>Al>Zn)大小关系有①_____②_____③_____.
(2)某钢铁厂用含杂质20%的赤铁矿石(主要成分是Fe2O3)冶炼生铁,若日产含铁96%的生铁140吨,要用赤铁矿石_____吨。
【答案】Al=Mg=Zn Al>Mg>Zn Al=Mg>Zn 240
【解析】
(1)每24份质量的镁会与73份质量的盐酸反应生成2份质量的氢气,每54份质量的铝和219份质量的盐酸反应生成6份质量的氢气,每65份质量锌和73份质量的盐酸反应生成2份质量的氢气,假设金属的质量都是24g,等质量的金属消耗盐酸的质量分别是:
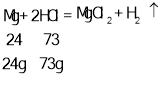
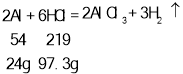
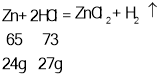
令三种金属质量均为24g,则
当盐酸质量m>73g时,生成氢气的质量:Al>Mg>Zn;
当盐酸质量27g<m≤73g时,生成氢气质量:Al=Mg>Zn;
当盐酸质量m≤27g时,生成氢气质量:Al=Mg=Zn
(2)设若日产含铁96%的生铁140吨,要用赤铁矿石的质量为x

![]() 解得:x=240t
解得:x=240t

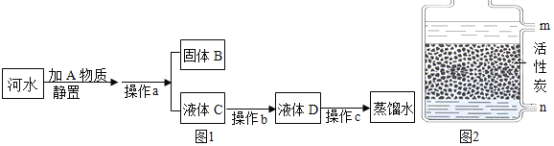
【题目】化学学习小组的同学们在用如图所示装置做木炭还原氧化铜实验时。发现试管中足量的澄清石灰水变浑浊,且有气泡不断冒出,于是同学们得出“木炭和氧化铜反应有二氧化碳生成”的结论。
小明同学提出如下质疑:
①木炭在高温下与试管内空气中的氧气反应也能产生二氧化碳,那么,澄清的石灰水变浑浊,不能说明二氧化碳一定是木炭和氧化铜反应产生的。
②石灰水中不断有气泡冒出,是什么气体呢?
根据小明的质疑,同学们进行了如下探究:
探究一:碳能否与氧化铜反应产生二氧化碳。
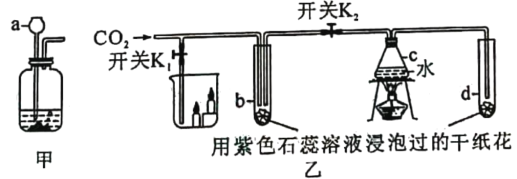
(设计实验)同学们将上述装置进行改进,设计了如甲图装置进行实验:
(主要实验步骤)
(1)组装仪器,检查装置的气密性。
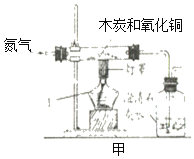
(2)在硬质玻璃管中装入氧化铜和木炭粉的混合物,集气瓶中放入足量澄清石灰水。
(3)通入一会儿氮气,目的是_____。再加热,酒精灯加网罩的作用是_____,观察现象。硬质玻璃管中的现象是_____。澄清的石灰水变浑浊。
(得出结论)碳能与氧化铜反应产生二氧化碳。
探究二:石灰水中不断冒出的是什么气体?
(猜想和假设)猜想一:CO2 猜想二:CO 猜想三:_____。
(查阅资料)CO气体能使湿润的黄色氯化钯试纸变蓝色。
(设计实验)根据各自的猜想,他们共同设计了如图乙所示的装置进行探究:装置A中放入一定比例的木炭粉和氧化铜的混合物,B、C中均放入澄清的石灰水,且B中石灰水保证足量,D中放入湿润的氯化钯试纸。
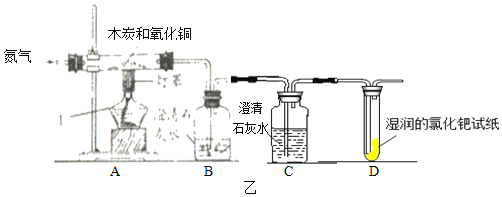
(现象与分析)
现象 | 结论 |
_____。 | 猜想三正确 |
(反思)
(1)同学们对CO产生的原因进行了
①原因一:木炭和氧化铜在高温条件下直接发生反出产生CO;
②原因二:反应C+2CuO![]() 2Cu+CO2↑中的一种产物和反应物木炭又发生了化学反应,产生了CO;
2Cu+CO2↑中的一种产物和反应物木炭又发生了化学反应,产生了CO;
请你从原因一、原因二中选择其一,用化学方程式表示存在此原因的化学反应原理_____。
由此,同学们想到乙图装置设计中存在缺陷,改进方法是_____。
(2)上图装置乙中B瓶中放入足量澄清石灰水,完全可以吸收装置A中产生的二氧化碳,为什么B瓶中冒出的气体还含有二氧化碳呢?同学们经过讨论认识到:A中溢出的气体气流比较急,且导管较细,部分生成的二氧化碳未与石灰水反应,便在气流的作用下溢出了。