题目内容
【题目】同学们在学习了木炭还原氧化铜的实验后,联想到单质碳的一些化学性质,对反应后的气体成分产生了疑问,某学习小组对该反应产物中的气体成分进行了探究。
〔猜想〕
①气体产物全部是CO2 ②气体产物全部是CO ③气体产物 ;
〔查阅资料〕 CO气体能使湿润的黄色氯化钯试纸变蓝色。
〔设计实验〕根据各自的猜想,他们共同设计了如下图的实验装置进行探究。
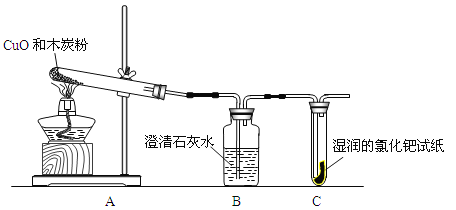
〔现象与分析〕
现象 | 结论 |
如果装置B , 装置C无现象 | 则猜想①成立 |
如果装置B无现象,装置C | 则猜想②成立 |
如果装置B ,装置C____________ | 则猜想③成立 |
〔结论〕实验现象证明猜想③成立,同学们的疑问是合理的。
〔反思〕
(1)同学们对CO产生的原因进行了分析:
①原因一:木炭和氧化铜在高温条件下直接发生反出产生CO;
②原因二:反应C+2CuO![]() 2Cu+CO2↑中的一种产物和反应物木炭又发生了化学反应,产生了CO;请你从原因一、原因二中选择其一,用化学方程式表示存在此原因的化学反应原理___________。
2Cu+CO2↑中的一种产物和反应物木炭又发生了化学反应,产生了CO;请你从原因一、原因二中选择其一,用化学方程式表示存在此原因的化学反应原理___________。
(2)根据上述实验,请你归纳出单质碳在工业上的重要用途 。
【答案】〔猜 想〕CO和二氧化碳
〔现象与分析〕
现象 | 结论 |
如果装置B澄清石灰水变浑浊 , 装置C无现象 | 则猜想①成立 |
如果装置B无现象,装置C试纸由黄色变为蓝色 | 则猜想②成立 |
如果装置B澄清石灰水变浑浊,装置C试纸由黄色变为蓝色 | 则猜想③成立 |
〔反思〕
(1)CO2+C点燃2CO 或 CuO+C加热Cu+CO
(2)冶炼金属
【解析】
试题分析:根据猜想1和猜想2综合考虑,可知气体产物可能是CO和二氧化碳的混合气体;根据资料和实验结论分析:若猜想①成立,则气体产物全部是CO2,现象为装置B澄清石灰水变浑浊,装置C无现象;猜想②成立,则气体产物全部是CO,现象为装置B无现象,装置C试纸由黄色变为蓝色;若猜想③成立,则气体产物是CO和二氧化碳的混合气体,现象为装置B澄清石灰水变浑浊,装置C试纸由黄色变为蓝色。木炭和氧化铜在高温条件下直接发生反出产生CO的化学方程式为CuO+C加热Cu+CO ,反应C+2CuO加热2Cu+CO2↑的产物中只有二氧化碳能与碳反应,即CO2+C点燃2CO ;根据上述实验可知碳具有还原性,则可利用这个性质来冶炼金属。