题目内容
【题目】汕头是滨海城市,盛产海盐。食盐是生活必需品,也是重要的化工原料。
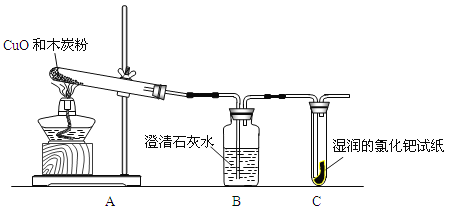
(1)某学习小组进行粗盐提纯实验,主要经过以下操作步骤:称量→溶解→ →蒸发→再次称量→计算产率。在蒸发操作中使用到玻璃棒,作用是 。实验结束后,该小组发现所得食盐产率明显低于其他小组,其原因可能是 。
A.粗盐未充分溶解就过滤
B.倾倒时,有部分氯化钠溶液溅出
C.蒸发后,所得的精盐较潮湿
(2)电解饱和食盐水可以得到多种化工产品,主要过程如下:
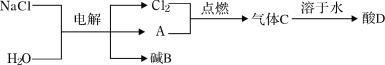
①气体A是密度最小的气体,该气体的名称为 ,写出一个由酸D转化为气体A 的化学方程式 。
②电解后生成的碱B的化学式为 ,你猜想的依据是 。
【答案】(1)过滤 搅拌,使之受热均匀,防止液滴飞溅 AB
(2)①氢气 Zn+2HCl=ZnCl2+H2↑
②NaOH 化学反应前后元素种类不变(或质量守恒定律)
【解析】
试题分析:(1)粗盐提纯实验,主要经过以下操作步骤:称量→溶解→过滤→蒸发→再次称量→计算产率;在蒸发操作中使用到玻璃棒,作用是:搅拌,使之受热均匀,防止液滴飞溅;发现所得食盐产率明显低的原因:A、粗盐未充分溶解就过滤,使得最终所得的精盐质量减少,产率偏低,正确,B、倾倒时,有部分氯化钠溶液溅出,氯化钠溶液中溶有溶质氯化钠,所以最终也会使得最终所得的精盐质量减少,产率偏低,正确,C、蒸发后,所得的精盐较潮湿,使得精盐质量偏大,产率也偏大,错误,故选AB
(2)①气体A是密度最小的气体,该气体的名称为氢气;D是一种酸,A是氢气,故一个由酸D转化为气体A的化学方程式:Zn+2HCl=ZnCl2+H2↑等
②碱是由金属离子和酸根离子构成,结合质量守恒定律,化学反应前后,元素的种类不变,故电解后生成的碱B的化学式为NaOH ;猜想的依据是:化学反应前后元素种类不变(或质量守恒定律)

 名校课堂系列答案
名校课堂系列答案