题目内容
某兴趣小组的同学在老师的指导下,对一瓶没有塞橡皮塞的氢氧化钙溶液进行探究,请你一起参与。
【提出问题】该氢氧化钙溶液是否全部变质?
【猜想与假设】猜想①:氢氧化钙溶液可能全部变质,变成碳酸钙。
猜想②:氢氧化钙溶液可能部分变质,其成分是 。
【实验探究】
| 实验步骤 | 实验现象 | 实验结论 |
| (1)取样于试管中,滴加稀盐酸,充分振荡 | 有 生成 | 原溶液中一定含有碳酸钙 |
| (2)另取样于试管中,滴加酚酞试液 | 溶液呈红色 | 原溶液中含有 |
【实验结论】综合上述实验(1)、(2),你得出的结论是猜想 成立。
【反思与拓展】(1)氢氧化钙露置于空气中容易变质,原因是 (用化学方程式表示)。
(2)在分析化学反应后的物质成分时,除了考虑生成物外,还需考虑的是 。
【猜想与假设】碳酸钙和氢氧化钙[或CaCO3和Ca(OH)2]
【实验探究】(1)无色气体 (2)氢氧化钙[或Ca(OH)2]
【实验结论】②
【反思与拓展】(1)CO2+Ca(OH)2=CaCO3↓+H2O
(2)反应物是否有剩余(或反应物是否反应完全等)
解析

(8分)(1)小方用下图所示装置对二氧化碳的灭火实验进行研究,
观察到的现象是____________________________________。
实验的结论是______________________________________。
(2)【提出问题】二氧化碳能否支持燃烧?
【猜想假设】镁能在二氧化碳中燃烧。
【查阅资料】①氧化镁、氢氧化镁均是白色难溶于水的固体。
②MgO+2HCl= MgCl2+H2O 、
③MgCl2+2NaOH=Mg(OH)2↓+2NaCl 。
【实验探究】
①下图中镁带剧烈燃烧,冒白烟,有黑色固体生成,并放出大量的热。
②为检验生成物的成分,做如下实验。
| 实验步骤 | 实验现象 | 实验结论和化学方程式 | |
| 向广口瓶中加入过量盐酸,充分反应后过滤,在滤纸上留有黑色固体。 | I、将黑色固体收集、洗涤、干燥后,点燃,在火焰上方罩一个蘸有澄清石灰水的烧杯。 | 黑色固体燃烧,烧杯内壁出现白色浑浊。 | 黑色固体是______; 反应的化学方程式是: ___________________。 |
| II、取少量滤液于试管中,逐滴加入氢氧化钠溶液。 | 开始_______,后有白色沉淀产生。 | 白烟的成分是______。 | |
③为了回收II中的白色沉淀,证明沉淀完全的实验方法是______________________
___________________________________(要求写出步骤、试剂、现象和结论)。
【反思提高】实验室中由某些活泼金属引起的着火,不能用二氧化碳灭火,应用细沙灭火。
一次性塑料包装袋造成的环境污染已经引起社会的高度关注,许多城市已经开始推广使用纸制食品袋。同学们经查阅资料得知,纸袋的组成成分中一定含有碳元素和氢元素,可能含有氧元素,于是他们利用以下装置进行实验测定。请回答下列问题: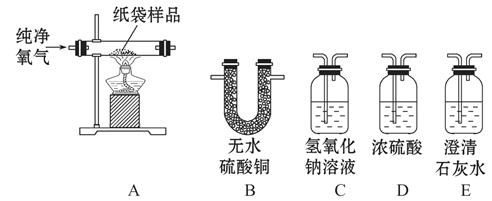
(1)实验中C装置内发生反应的化学方程式为 。
(2)实验中选择纯净的氧气而不用空气的原因是 。
(3)为分别吸收纸袋充分燃烧的产物,并通过清晰可见的现象检验吸收是否安全高效,以上实验装置正确的连接顺序是A→( )→( )→( )→( )(填写装置的字母代号)
(4)将实验装置正确连接之后,确认气密性良好,充分燃烧16.2 g纸袋样品,测得相关实验数据见表(假定燃烧产物被完全吸收,灰烬质量忽略不计)
| 装置 | 实验前装置的质量 | 实验后装置的质量 |
| B | 200.0 g | 200.0 g |
| C | 210.0 g | 234.2 g |
| D | 220.0 g | 229.0 g |
| E | 210.0 g | 212.2 g |
通过分析和计算可推断得出,纸袋样品中 (填“含”或“不含”)氧元素,其碳、氢两种元素的原子个数的最简整数比为 。
通过实验对草酸(相对分子质量是90)进行如下研究。
【查阅资料】①浓硫酸常作干燥剂 ②浓NaOH溶液常用于吸收CO2气体
③无水硫酸铜吸水后由白色变为蓝色 ④氯化钯(PdCl2)溶液遇CO产生黑色沉淀
【实验准备】选用下列实验装置(气密性良好,部分固定装置已略去):
【实验I】检验草酸分解的产物。
| 实验步骤 | 实验现象 | 实验结论及分析 |
| (1)按A→H→E→C 连接仪器 (2)关闭K,点燃A处酒精灯 | H中 E中澄清石灰水变浑浊 C中产生黑色沉淀,气球鼓起 | 草酸分解生成了CO2、CO和H2O ①E中反应的化学方程式是 ②C中气球的作用是 |
【实验II】取9 g草酸进行实验,测定生成物的质量并确定草酸的组成。
| 实验步骤 | 实验数据 | 实验结论及分析 |
| (1)选择A、B、D、G装置组合进行实验 (2)鼓入过量的N2后,分别称量B、D、G的质量 (3)关闭K,点燃A、D处的酒精灯,至草酸完全分解 (4)熄灭A处酒精灯,通入过量的N2,熄灭D处酒精灯,再次分别称量B、D、G的质量 | B装置增重1.8 g D装置中固体质量减少0.8 g G装置增重4.4 g | ①A、B、D、G装置的正确连接顺序是A→ → →D ②向A中两次通入N2,其中 第二次的目的是 ③草酸的化学式是 ④反思:若用F代替B,则不能测定草酸的组成,其原因是 |