题目内容
【题目】静宁县治平乡鞍子山峡盛产石灰石,为了测定此地石灰石中碳酸钙的质量分数,某学校兴趣小组的同学称取石灰石样品12.5g,高温煅烧至质量不再改变,称得剩余固体质量为8.1g(假设杂质不参加反应;发生反应的化学方程式为CaCO3![]() CaO+CO2↑ ),试计算:
CaO+CO2↑ ),试计算:
(1)生成二氧化碳质量是 g;
(2)石灰石样品中碳酸钙的质量分数是多少?(写出计算过程)
【答案】(1)4.4;(2)80%
【解析】(1)生成二氧化碳的质量为:12.5g﹣8.1g=4.4g;
(2)设碳酸钙的质量为x.
CaCO3![]() CaO+CO2↑
CaO+CO2↑
100 44
x 4.4g
![]() =
=![]()
x=10 g
石灰石样品中碳酸钙的质量分数为:![]() ×100%=80%
×100%=80%
答:石灰石样品中碳酸钙的质量分数是80%.

【题目】某课外活动小组在学习了书本“空气中氧气含量的测定”实验,知道P2O5不能随便排放在空气中,否则会对空气造成污染,所以对该实验进行了改进:
如图所示:在由两个注射器组成的密闭系统内共有25mL空气,然后给装有红磷的玻璃管加热.同时交替推动两个注射器的活塞,至玻璃管内的红磷变成白烟,且较长时间内无进一步变化后停止加热,待冷却至室温,将气体全部推至一个注射器内.回答下列问题:
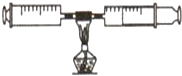
(1)在实验的加热过程中,交替缓慢推动两个注射器的目是 .
(2)写出红磷燃烧的化学反应方程式 .
(3)小组测得实验结果如下:
反应前注射器内气体总体积 | 反应后注射器内气体总体积 |
25mL | 22mL |
由此数据可以推算出他测定的空气中氧气的体积分数 2l%(填“>”、“=”“<”)
造成该实验出现误差的原因可能是 (填序号).
A.没有交替缓缓推动两个注射器活塞;
B.读数时没有冷却至室温;
C.加入红磷量太少;
D.装置漏气
(4)通过上面的实验,你学到的测量混合物中某成分含量的方法是 .