题目内容
【题目】实验课上,同学们利用下列装置进行气体制备的学习,请回答下列问题:
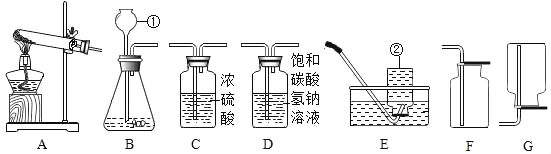
(1)写出编号的仪器名称:①_____,②_____。
(2)写出用A装置制取氧气反应的化学方程式_____,收集装置是_____。
(3)若要制取一瓶纯净、干燥的二氧化碳气体,装置连接的正确顺序是_____→D→C→F,D装置的作用是_____。
(4)现用收集的二氧化碳进行实验,探究CO2与NaOH溶液发生的反应。(提示;Ca(OH)2微溶于水)
①实验一:小雨取一充满CO2的矿泉水瓶,加入一定量的水,立即拧紧瓶盖,振荡,发现瓶子变瘪;小雨另取一相同的充满CO2的矿泉水瓶向其中加入与水等体积的NaOH溶液,立即拧紧瓶盖,振荡,得到溶液X,此时观察到的现象是_____。实验中,小雨采用两只矿泉水瓶做对比实验的目的是_____。
②实验二:为检验CO2与NaOH溶液反应的产物,小亮取实验一所得溶液X少许,向其中滴加BaC12溶液,有白色沉淀产生,该反应的化学方程式:_____,实验中不宜将BaCl2溶液换成CaCl2溶液的原因是_____。
【答案】长颈漏斗 集气瓶 2KMnO4![]() K2MnO4+MnO2+O2↑ E或F B 除去二氧化碳中混有的氯化氢气体 倒入NaOH溶液的塑料瓶比倒入水的塑料瓶瘪 使用塑料瓶,现象比较明显 Na2CO3+BaCl2=BaCO3↓+2NaCl 因为如果氢氧化钠溶液有剩余,形成的氢氧化钙微溶于水,也会有白色沉淀
K2MnO4+MnO2+O2↑ E或F B 除去二氧化碳中混有的氯化氢气体 倒入NaOH溶液的塑料瓶比倒入水的塑料瓶瘪 使用塑料瓶,现象比较明显 Na2CO3+BaCl2=BaCO3↓+2NaCl 因为如果氢氧化钠溶液有剩余,形成的氢氧化钙微溶于水,也会有白色沉淀
【解析】
(1)仪器①是长颈漏斗,②是集气瓶;故填:长颈漏斗;集气瓶;
(2)装置A适用于固体加热制取氧气,试管口处有棉花团,所以是加热高锰酸钾制取氧气,同时生成锰酸钾和二氧化锰;氧气的密度比空气大,不易溶于水,所以可用向上排空气法或排水法来收集;故填:2KMnO4![]() K2MnO4+MnO2+O2↑;E或F;
K2MnO4+MnO2+O2↑;E或F;
(3)实验室制取二氧化碳属于固液常温型,选择装置B来制取,气体提纯的一般思路是:先除杂质后干燥,并且是长进短出;二氧化碳中的杂质氯化氢气体一般用碳酸氢钠溶液来吸收,一般用浓硫酸进行干燥,二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集,因此这套装置的连接顺序应是B→D→C→F;碳酸氢钠溶液可以除去二氧化碳中混有的氯化氢气体;故填:B;除去二氧化碳中混有的氯化氢气体;
(4)①氢氧化钠和二氧化碳反应生成碳酸钠和水,所以实验一,观察到的现象是:倒入NaOH溶液的塑料瓶比倒入水的塑料瓶瘪;实验中,小雨采用两只矿泉水瓶做对比实验的目的是:使用塑料瓶,现象比较明显;故填:倒入NaOH溶液的塑料瓶比倒入水的塑料瓶瘪;使用塑料瓶,现象比较明显;
②实验二中,碳酸钠和氯化钡反应生成碳酸钡白色沉淀和氯化钠,化学方程式为:Na2CO3+BaCl2=BaCO3↓+2NaCl;实验中不宜将BaCl2溶液换成CaCl2溶液的原因是:因为如果氢氧化钠溶液有剩余,形成的氢氧化钙微溶于水,也会有白色沉淀;故填:Na2CO3+BaCl2=BaCO3↓+2NaCl;因为如果氢氧化钠溶液有剩余,形成的氢氧化钙微溶于水,也会有白色沉淀。

 阅读快车系列答案
阅读快车系列答案【题目】20℃时,在盛有 100g 水的烧杯中加入 70g 硝酸钾,充分溶解后,逐渐升温(不 考虑水蒸发的影响),测定不同温度时剩余固体质量。测定结果记录如下表:
溶液温度/℃ | 20 | 30 | 40 | 50 | 60 |
剩余固体质量/g | 38.4 | 24.2 | 6.1 | 0 | 0 |
(1)20℃时,硝酸钾的溶解度为_____。
(2)30℃时,所得溶液是硝酸钾的_____(填“饱和”或“不饱和”)溶液,该溶液中硝酸钾 的质量分数为_____(结果保留到 0.1%)
(3)温度从 50℃升高到 60℃过程中,溶液中硝酸钾的质量分数_____(填字母)。
A 变大 B 变小 C 不变 D 无法判断
(4)将 60℃时接近饱和的硝酸钾溶液变成饱和溶液,下列方法能达到目的有_____(填字母)。
a 升温 b 降温 c 加适量硝酸钾 d 加适量水 e 恒温蒸发水
(5)某同学要配制 50g 溶质质量分数为 15%的硝酸钾溶液,实验时发现硝酸钾已结块,为 了较快地溶解,合理的方法有_____(填字母)。
A将硝酸钾研碎 B 用热水溶解 C 多加一些水 D 用玻璃棒搅拌