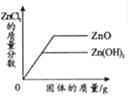题目内容
【题目】金属材料的研究和应用是化学学习的一个重要内容.
(1)利用铝的 性可将铝块制成铝箔.
(2)工业上用一氧化碳还原赤铁矿冶炼金属铁的化学方程式为 .
(3)因生铁和钢的 不同,导致它们在性能上有很大差异.
(4)验证铝、铜、银的活动性顺序时,除铝、银外还需要用到的一种试剂是 ,除此之外,还可以通过它们与氧气反应的 比较它们的活泼性.
【答案】(1) 延展;(2)Fe2O3+3CO![]() 2Fe+3CO2;(3)含碳量;
2Fe+3CO2;(3)含碳量;
(4)硫酸铜溶液(或其他可溶性的铜盐溶液);剧烈程度。
【解析】
试题分析:(1)利用金属铝具有良好的延展性可把金属铝制成片;
(2)工业上用一氧化碳还原氧化铁炼铁,主要是利用CO的还原性,在高温下和氧化铁反应生成铁和二氧化碳,反应的化学方程式为Fe2O3+3CO![]() 2Fe+3CO2;
2Fe+3CO2;
(3)生铁和钢在性能上有很大差异是因为含碳量不同,其中生铁的含碳量高;
(4)验证铝、铜、银的活动性顺序时,除铝、银外还需要用到可溶性铜盐溶液,因为铝可知置换出铜,而银不能,从而证明了铝的活动性大于铜,铜的活动性大于银;除此之外,还可以通过它们与氧气反应的剧烈程度来判断.铝能在氧气中剧烈燃烧;而铜能与氧气在加热的条件下反应,银不与氧气反应。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
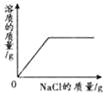
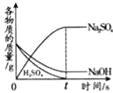
【题目】如表中,有关量的变化图象与其对应叙述相符的是( )
A | B | C | D |
|
|
|
|
向接近饱和的NaCl溶液中加入固体NaCl | 向等质量、等质量分数的两份稀盐酸中分别加入足量的ZnO和Zn(OH)2 | 向Na2CO3溶液中加入一定溶质质量分数的NaOH溶液 | 等质量、等质量分数的H2SO4溶液与NaOH溶液混合 |
A.A B.B C.C D.D