题目内容
【题目】根据下图回答问题: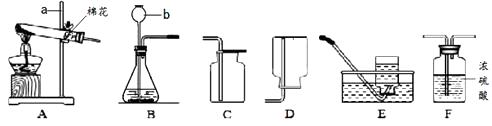
(1)仪器a和b的名称分别是、。
(2)实验室若用A装置来制取氧气,反应的化学方程式为 , 你选用的一种收集装置是(填字母,下同),选择的理由是。
(3)在实验室里,可用亚硫酸钠(Na2SO3)固体和稀硫酸的反应来制取SO2气体,该反应的化学方程式为。在通常情况下SO2是一种无色、有刺激性气味的有毒气体,能溶于水且水溶液呈酸性。实验室制取并收集纯净干燥的SO2(在通风橱中进行)应选用的装置组合是。收集好后,多余的SO2气体可用F装置来吸收,此时应把里面浓硫酸换成溶液。
【答案】
(1)铁架台,长颈漏斗
(2)2KMnO4 ![]() K2MnO4+MnO2+O2↑,C,氧气的密度比空气大(或E,氧气不易溶于水)
K2MnO4+MnO2+O2↑,C,氧气的密度比空气大(或E,氧气不易溶于水)
(3)Na2SO3+H2SO4=Na2SO4+H2O+SO2↑,BFC,NaOH
【解析】解:(1)根据已学知识仪器a和b的名称分别是铁架台,长颈漏斗;(2)用A装置制取氧气,是加热高锰酸钾制取氧气,方程式为2KMnO4 ![]() K2MnO4+MnO2+O2↑;氧气的密度比空气大,可用向上排空气法即C;(3)亚硫酸钠(Na2SO3)固体和稀硫酸的反应来制取SO2气体,类似制CO2,故方程式为Na2SO3+H2SO4=Na2SO4+H2O+SO2↑,依题意装置为BFC;碱可以与SO2反应即可用NaOH。
K2MnO4+MnO2+O2↑;氧气的密度比空气大,可用向上排空气法即C;(3)亚硫酸钠(Na2SO3)固体和稀硫酸的反应来制取SO2气体,类似制CO2,故方程式为Na2SO3+H2SO4=Na2SO4+H2O+SO2↑,依题意装置为BFC;碱可以与SO2反应即可用NaOH。
所以答案是:(1)铁架台,长颈漏斗,(2)2KMnO4 ![]() K2MnO4+MnO2+O2↑;C;氧气的密度比空气大(或E,氧气不易溶于水);(3)Na2SO3+H2SO4=Na2SO4+H2O+SO2↑;BFC;NaOH。
K2MnO4+MnO2+O2↑;C;氧气的密度比空气大(或E,氧气不易溶于水);(3)Na2SO3+H2SO4=Na2SO4+H2O+SO2↑;BFC;NaOH。
【考点精析】本题主要考查了氧气的收集方法的相关知识点,需要掌握收集装置:根据物质的密度、溶解性;排水法收集时,待气泡均匀连续冒出时再收集(刚开始排出的是试管中的空气;)用排空气法收集气体时,导管伸到集气瓶底部才能正确解答此题.

【题目】如图所示的暖宝宝是一种防寒用品。小明想知道暖宝宝中的主要成分有哪些?暖宝宝发热的原因是什么?
小明探究:暖宝宝中的主要成分是什么?
剪开内包装袋,倒出其中的粉末,发现呈黑色。
【提出猜想】该黑色粉末可能含有木炭粉、铁粉、氧化铜中的一种或几种。
【初步验证】将磁铁靠近黑色粉末,部分被吸引。
(1)【得出结论】该黑色粉末中一定含有 , 可能含有。
(2)【查阅资料】木炭与稀硫酸不反应,氧化铜与稀硫酸反应能产生蓝色溶液。
【进行实验】
实验编号 | 实验操作 | 实验现象 |
① | 取少量黑色粉末于试管中,加足量稀硫酸 | 固体部分溶解,有气泡产生,溶液未变蓝色 |
② | 取实验①的残渣灼烧,将内壁涂有澄清石灰水的小烧杯罩在上方 | 澄清石灰水变浑浊 |
由实验①可知,该黑色粉末中一定含有 , 一定不含。
写出实验①的化学反应方程式。
由实验②可知,该黑色粉末中一定含有。
(3)小明思考:暖宝宝为什么会发热?
【网络资料】暖宝宝中除含有铁粉、木炭外,还含有食盐和水。
①暖宝宝贴在衣服上与空气接触后会发热的原因是
②由此可见,人们可以利用化学反应放出的能量,请再举一例: .
请你猜测暖宝宝中氯化钠的作用是。
