题目内容
【题目】(12分)定量研究对于化学科学发展有重大作用,因此我们应该掌握好有关质量守恒定律的相关知识。
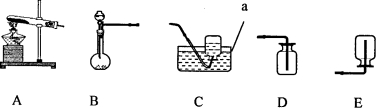
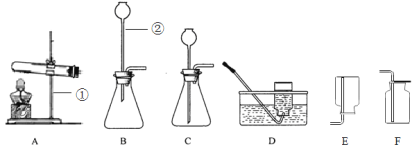
(1)下图A、B、C三个实验用于验证质量守恒定律,其中不能达到实验目的的是 (选填序号),理由是 。
(2)自然界中绿色植物光合作用可用下式表示:CO2 + H2O![]() 淀粉 + O2
淀粉 + O2
① 分析化学反应前后元素种类可知:淀粉中一定含有的元素是_ ___(填元素符号),可能含有的元素是__ _ _(填名称)。
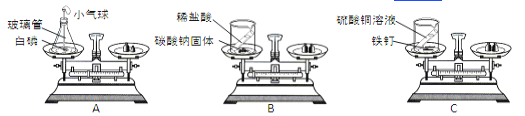
在一个密闭容器内有A、B、C、D四种物质,在一定条件下充分反应,测得反应前后各物质的质量如下表:
物质 | A | B | C | D |
反应前质量/g | 2 | 24.5 | 4 | 8 |
反应后质量/g | 16.9 | 0 | 13.6 | X |
表中X=________,在反应中D这种物质可能起_ __ _ 作用。容器内发生反应的基本类型是________。
(3)某兴趣小组为验证质量守恒定律,做了镁条在空气中燃烧的实验。
①请写出镁条与氧气反应的文字表达式_ __ _。
②小明发现燃烧后产物的质量大于反应物镁条的质量,认为这个反应不遵循质量守恒定律。小红对此提出了异议,小红的理由是_ __ _。
(4)右图是一个具有刻度和可滑动的活塞的玻璃容器,其中有空气和足量的白磷,将它放在盛有沸水的烧杯上方,进行实验。请回答下列问题:
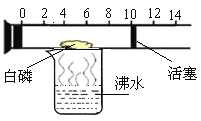
①玻璃容器中发生反应的文字表达式为: 。
实验目的 | 实验现象 | 实验结论 |
测定空气中 的体积分数 | 白磷着火燃烧,活塞先右移,后左移,最后停在刻度约为 (填整数)的位置上。 | 空气的成分按体积计算,该气体约占空气体积的21% |
②填写表格中的空白:
【答案】(1)B 生成的气体逸出(或没有在密闭容器中进行反应)
(2)①C、H(或碳、氢)(有错、漏均不得分) 氧元素
②8 催化 分解反应(只写“分解”不得分)
(3)①镁 + 氧气![]() 氧化镁
氧化镁
②任何化学反应都符合质量守恒定律,该反应前后质量不相等的原因是空气中氧气参加了反应(意思对即可得分)
(4)①磷 + 氧气![]() 五氧化二磷;
五氧化二磷;
②氧气 8
【解析】
试题分析:(1)A在密闭环境中进行,可以用于验证质量守恒定律;B反应产生气体,却是在敞口状态下进行,故不能用于验证质量守恒定律;C反应没有气体参加反应,故可以再敞口状态下进行,可以用于验证质量守恒定律。故选B。
(2)①根据质量守恒定律,反应物中有C、H、O三种元素,生成物中也应该含有这三种元素,故淀粉中一定有C、H两种元素,可能含有氧元素。
②此反应是在密闭环境中进行,故根据质量守恒定律,可知反应前后物质的总质量不变,故2+24.5+4+8=16.9+0+13.6+X,X=8;反应前后D的质量不变,可能是催化剂,起催化作用;比较反应前后物质的质量,可知B为反应物,A、C为生成物,故反应类型为:分解反应。
(3)①镁条在氧气中燃烧生成氧化镁,反应的文字表达式为:镁 + 氧气![]() 氧化镁
氧化镁
②任何化学反应都符合质量守恒定律,对于这个化学反应,参加反应的镁的质量与氧气的质量和等于生成氧化镁的质量。该反应前后质量不相等的原因是空气中氧气参加了反应,而称量时未计算氧气的质量。
(4)①白磷着火点较低,温度达到时它会与空气中的氧气反应生成五氧化二磷,反应的文字表达式为:磷 + 氧气![]() 五氧化二磷;
五氧化二磷;
②这个实验是为了测定空气中氧气的体积分数;氧气约占空气体积的20%,故反应后活塞大约停在刻度8处。

 53随堂测系列答案
53随堂测系列答案【题目】元素周期表是学习和研究化学的重要工具,它的内容十分丰富。下表是元素周期表的部分内容,请认真分析并回答后面的问题:
IA | 0 | ||||||||
1 | 1 氢 1.008 | 2 He 氦 4.003 | |||||||
IIA | IIIA | IVA | VA | VIA | VIIA | ||||
2 | 3 Li 锂 6.941 | 4 Be 铍 9.012 | 5 B 硼 10.81 | 6 C 碳 12.01 | 7 N 氮 14.01 | 8 O 氧 16.00 | 9 F 氟 19.00 | 10 Ne 氖 20.18 | |
3 | 11 Na 钠 22.99 | 12 Mg 镁 24.31 | 13 Al 铝 26.98 | 14 Si 硅 28./span>09 | 15 P 磷 30.97 | 16 S 硫 32.06 | 17 Cl 氯 35.45 | 18 Ar 氩 39.95 | |
(1)请从上表中查出地壳中含量最多的金属元素的相对原子质量为
(2)表中不同种元素最本质的区别是 (填序号):
A.相对原子质量不同 B.质子数不同 C.中子数不同
(3)元素周期表中每一个横行叫做一个周期,通过分析,同一周期元素之间的排列有一定的规律,下列规律中不正确的是: (填字母序号)
A.从左到右,各元素原子的电子层数相同
B.从左到右,各元素原子的原子序数依次增加
C.从左到右,各元素原子的最外层电子数相同
D.从左到右,由金属元素逐渐向非金属元素过渡
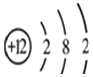
(4)元素周期表中,原子序数为12的镁元素的原子结构示意图如图,该原子在化学反应中易 (填 “得到”或“失去”)电子.说明元素的化学性质与原子的关系密切.