题目内容
(4分)请用“﹤”、“﹥”或“﹦”填空。
(1)相同条件下在水中的溶解性:氢氧化钙 氢氧化钠;
(2)含碳量:生铁 钢;
(3)pH:硫酸溶液 氢氧化钠溶液;
(4)氢原子核内质子数 氢原子核外电子数。
(1)﹤ (2)﹥ (3)﹤ (4)﹦
解析试题分析:(1)氢氧化钙是微溶于水,而氢氧化钠是易溶于水,故相同条件下在水中的溶解性:氢氧化钙﹤氢氧化钠
(2)生铁和钢都是铁的合金,生铁含碳量2~4.3%,钢的含碳量0.03~2%,故含碳量:生铁﹥钢
(3)硫酸溶液显酸性,PH﹤7,氢氧化钠溶液显碱性,PH﹥7,故pH:硫酸溶液﹤氢氧化钠溶液
(4)在原子中,质子数=核外电子数,故氢原子核内质子数=氢原子核外电子数
考点:物质的溶解性,铁的合金,溶液的PH,原子的构成

练习册系列答案
相关题目
世界每年因腐蚀而报废的金属设备和材料相当于年产量的20% ~ 40% ,为探究铁锈蚀条件,某同学设计的实验如图所示,一周后观察到_______(填序号)试管内的铁钉生锈。请分析铁生锈的条件及防锈措施。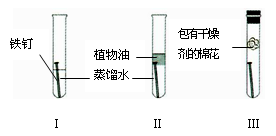
(7分)使用密度小、强度大的镁合金能减轻汽车自重,从而减少汽油消耗和废气排放。
|
(3)制镁的原料MgO可从海水中获得。小华利用镁与盐酸反应后的废液,模拟从海水中获取MgO的过程,实验如下:
步骤1:向上述废液中,边搅拌边分批加入CaO,至MgCl2完全沉淀为止,过滤得Mg(OH)2固体。共消耗8.4g CaO。
步骤2:将Mg(OH)2固体加热分解为MgO和水,所得MgO的质量为4.0g 。
①步骤2中Mg(OH)2分解的化学方程式为 。
②通过所得MgO的质量计算上述废液中含MgCl2的质量m= g。
③分析实验数据,可知步骤Ⅰ中反生的化学反应有:
CaO+H2O==Ca(OH)2;Ca(OH)2+MgCl2==CaCl2+Mg(OH)2↓; 。
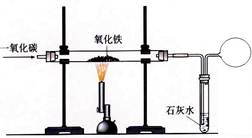
在反应:3CO+Fe2O3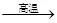 2Fe+3CO2中,还原剂是
2Fe+3CO2中,还原剂是
| A.CO | B.Fe2O3 | C.Fe | D.CO2 |