题目内容
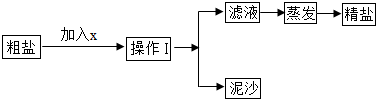
为了除去粗盐配制成的NaCl溶液中所含有的少量MgCl2,CaCl2和MgSO4杂质,某同学从碳酸钠溶液、稀盐酸、硝酸钡溶液、碳酸钾溶液和氢氧化钡溶液中选择了A、B、C三种试剂,按以下步骤进行了实验:
实验Ⅰ:向溶液中加入过量A后过滤得到滤液1;
实验Ⅱ:向滤液1中加过量B后过滤得到滤液2;
实验Ⅲ:向滤液2中加适量C,得到较纯净的NaCl溶液.
请回答下列问题:
①A、B、C三种试剂中溶质的化学式分别为______
②实验I中,所加A要过量的原因______
③实验II中,所加B要过量的原因______
④实验Ⅲ中,试剂加到______时为适量,此时得到较为纯净的NaCl溶液.
实验Ⅰ:向溶液中加入过量A后过滤得到滤液1;
实验Ⅱ:向滤液1中加过量B后过滤得到滤液2;
实验Ⅲ:向滤液2中加适量C,得到较纯净的NaCl溶液.
请回答下列问题:
①A、B、C三种试剂中溶质的化学式分别为______
②实验I中,所加A要过量的原因______
③实验II中,所加B要过量的原因______
④实验Ⅲ中,试剂加到______时为适量,此时得到较为纯净的NaCl溶液.
(1)要除去MgCl2、CaCl2和MgSO4杂质,就是除去Mg2+、Ca2+和SO42-,可以分别选用OH-、CO32-和Ba2+除去,选择的除杂试剂与杂质反应时要求不能生成新的杂质,后加的试剂能将上一步过量的试剂反应掉,可以选用的物质分别是氢氧化钡、碳酸钠、以及盐酸,所以本题答案为:Ba(OH)2、Na2CO3、HCl;
(2)为了充分除去Mg2+和SO42-,需要加入过量的氢氧化钡,氢氧化钡能与氯化镁反应生成氢氧化镁沉淀和氯化钡,硫酸镁能与氢氧化钡反应生活硫酸钡沉淀和氢氧化镁沉淀,所以本题答案为:为了除尽MgCl2、MgSO4;
(3)为了除去Ca2+和上一步过量的钡离子,需要加入过量的碳酸钠,碳酸钠能与氢氧化钡反应生成碳酸钡沉淀和氢氧化钠,能与氯化钙反应生成碳酸钙沉淀和氯化钠,能与氯化钡反应生成碳酸钡沉淀和氯化钠,所以本题答案为:为了除尽Ba(OH)2、CaCl2、BaCl2;
(4)经过实验Ⅰ和实验Ⅱ,食盐中还含有的杂质是氢氧化钠和碳酸钠,此时可以加入盐酸将多余的氢氧化钠和碳酸钠除掉,碳酸钠能与盐酸反应生成二氧化碳气体,当完全反应时无气泡产生,所以本题答案为:刚好无气体放出.
故答案为:(1)Ba(OH)2、Na2CO3、HCl;
(2)为了除尽MgCl2、MgSO4(或答:为了除尽Mg2+、SO42-);
(3)为了除尽Ba(OH)2、CaCl2、BaCl2(或答:为了除尽Ba2+、Ca2+);
(4)刚好无气体放出时(或答:用酚酞检验,红色刚刚褪去时).
(2)为了充分除去Mg2+和SO42-,需要加入过量的氢氧化钡,氢氧化钡能与氯化镁反应生成氢氧化镁沉淀和氯化钡,硫酸镁能与氢氧化钡反应生活硫酸钡沉淀和氢氧化镁沉淀,所以本题答案为:为了除尽MgCl2、MgSO4;
(3)为了除去Ca2+和上一步过量的钡离子,需要加入过量的碳酸钠,碳酸钠能与氢氧化钡反应生成碳酸钡沉淀和氢氧化钠,能与氯化钙反应生成碳酸钙沉淀和氯化钠,能与氯化钡反应生成碳酸钡沉淀和氯化钠,所以本题答案为:为了除尽Ba(OH)2、CaCl2、BaCl2;
(4)经过实验Ⅰ和实验Ⅱ,食盐中还含有的杂质是氢氧化钠和碳酸钠,此时可以加入盐酸将多余的氢氧化钠和碳酸钠除掉,碳酸钠能与盐酸反应生成二氧化碳气体,当完全反应时无气泡产生,所以本题答案为:刚好无气体放出.
故答案为:(1)Ba(OH)2、Na2CO3、HCl;
(2)为了除尽MgCl2、MgSO4(或答:为了除尽Mg2+、SO42-);
(3)为了除尽Ba(OH)2、CaCl2、BaCl2(或答:为了除尽Ba2+、Ca2+);
(4)刚好无气体放出时(或答:用酚酞检验,红色刚刚褪去时).

练习册系列答案
 名师金手指领衔课时系列答案
名师金手指领衔课时系列答案
相关题目