题目内容
(2011?吉林)同学们用Na2CO3溶液和浓HCl来研究简易灭火器的反应原理时,对废液的成分进行探究.[推理假设]
上述两种物质发生反应的化学方程式为______,由此推测出废液中一定有NaCl,可能有Na2CO3或盐酸.
[实验探究]
(一)确定废液中是否含有盐酸:
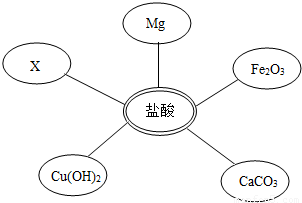
(1)选择试剂:根据盐酸的化学性质,同学们选用了如图所示的五种物质,其中物质x是酸碱指示剂中的______溶液.
(2)实验验证:某同学向废液中加入少量的镁粉,观察到______确定废液中一定没有盐酸.
(二)确定废液中是否含有Na2CO3某同学选用______测出废液的pH=l0,确定废液中一定含有Na2CO3.
(三)处理废液,回收利用欲从废液中得到纯净的NaCl,请完成如下实验方案设计.
| 方案 | 加入试剂 | 分离方法 | 方案评价 |
| 一 | 适量Ca(NO3)2溶液 | 过滤、蒸发结晶 | 不可行,理由是 ______ |
| 二 | 过量的______ | 蒸发结晶 | 可行 |
【答案】分析:[推理假设]根据碳酸钠与盐酸反应的实质写出其反应的化学方程式;
[实验探究]
(一)(1)判定废液中是否含盐酸所取用的酸碱指示剂不能用酚酞试剂,因酸不能使无色的酚酞变色;(2)明确镁和盐酸反应出现的现象;
(二)测定溶液的酸碱性的最简单方法用pH试纸;
(三)根据化学上除杂质原则分析实验方案设计,即除去原杂质不能添加新的杂质.
解答:解:[推理假设]根据碳酸钠与盐酸反应的实质写出其反应的化学方程式为:Na2CO3+2HCl=2NaCl+H2O+CO2↑;
[实验探究](一)
(1)判定废液中是否含盐酸所取用的酸碱指示剂不能用酚酞试剂,因酸不能使无色的酚酞变色,故取用石蕊试液,酸能使石蕊试液变红色;
(2)镁和盐酸反应出现的现象是产生大量气泡,如没气泡产生则证明废液中一定没有盐酸;
(二)测定溶液的酸碱性的最简单方法用pH试纸(也可使用pH计);
(三)根据化学上除杂质原则分析实验方案设计,即除去原杂质不能添加新的杂质,因而处理废液,回收利用废液中得到纯净的NaCl时,如加适量Ca(NO3)2溶液,虽然除去了碳酸钠,但却引进新杂质NaNO3;如加入过量的稀盐酸蒸发结晶后可得到纯净的氯化钠.
故答案为:
[推理假设]Na2CO3+2HCl=2NaCl+H2O+CO2↑
[实验探究]
(一)
(1)石蕊
(2)无气泡产生(或无现象或无变化)
(二)pH试纸(或pH计)
点评:此题考查探究酸的性质及书写有关化学方程式,题型设计科学合理,能很好的培养学生对酸的知识系统化,不再机械记忆,囫囵吞枣的记忆酸碱盐的知识点.
[实验探究]
(一)(1)判定废液中是否含盐酸所取用的酸碱指示剂不能用酚酞试剂,因酸不能使无色的酚酞变色;(2)明确镁和盐酸反应出现的现象;
(二)测定溶液的酸碱性的最简单方法用pH试纸;
(三)根据化学上除杂质原则分析实验方案设计,即除去原杂质不能添加新的杂质.
解答:解:[推理假设]根据碳酸钠与盐酸反应的实质写出其反应的化学方程式为:Na2CO3+2HCl=2NaCl+H2O+CO2↑;
[实验探究](一)
(1)判定废液中是否含盐酸所取用的酸碱指示剂不能用酚酞试剂,因酸不能使无色的酚酞变色,故取用石蕊试液,酸能使石蕊试液变红色;
(2)镁和盐酸反应出现的现象是产生大量气泡,如没气泡产生则证明废液中一定没有盐酸;
(二)测定溶液的酸碱性的最简单方法用pH试纸(也可使用pH计);
(三)根据化学上除杂质原则分析实验方案设计,即除去原杂质不能添加新的杂质,因而处理废液,回收利用废液中得到纯净的NaCl时,如加适量Ca(NO3)2溶液,虽然除去了碳酸钠,但却引进新杂质NaNO3;如加入过量的稀盐酸蒸发结晶后可得到纯净的氯化钠.
故答案为:
[推理假设]Na2CO3+2HCl=2NaCl+H2O+CO2↑
[实验探究]
(一)
(1)石蕊
(2)无气泡产生(或无现象或无变化)
(二)pH试纸(或pH计)
| 方案 | 加入试剂 | 分离方法 | 方案评价 |
| 引进新杂质(或有NaNO3,生成或引进NO3-) | |||
| 盐酸(或稀HCl或HCl) |
点评:此题考查探究酸的性质及书写有关化学方程式,题型设计科学合理,能很好的培养学生对酸的知识系统化,不再机械记忆,囫囵吞枣的记忆酸碱盐的知识点.

练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目
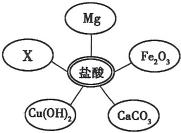 (2011?吉林)同学们用Na2CO3溶液和浓HCl来研究简易灭火器的反应原理时,对废液的成分进行探究.
(2011?吉林)同学们用Na2CO3溶液和浓HCl来研究简易灭火器的反应原理时,对废液的成分进行探究. (2011?大庆)同学们设计了如图所示装置来探究二氧化碳的制取和性质,下列关于该实验的叙述正确的是( )
(2011?大庆)同学们设计了如图所示装置来探究二氧化碳的制取和性质,下列关于该实验的叙述正确的是( )