题目内容
【题目】下列关于合金的说法不正确的是
A. 合金具有许多良好的物理、化学、机械性能
B. 合金的硬度一般比各成分金属大
C. 合金就是将不同的金属在高温下熔合而成
D. 多数合金的熔点比它的成分金属要低
【答案】C
【解析】
A、制合金的目的是将各种金属的优点加以利用,故正确
B、合金的硬度一般比组成合金的各成分硬度高,故B正确,
C、合金形成条件:其中任一金属的熔点不能高于另一金属的沸点.因为如果其中任一金属的熔点高于另一金属的沸点时,当任一金属的温度达到熔点熔化时,另一金属的温度已经达到沸点,开始沸腾蒸发,不能有效地形成合金,故错误
D、合金的熔点比各成分的熔点低,故D正确,
故选C.

练习册系列答案
 53随堂测系列答案
53随堂测系列答案
相关题目
【题目】(一)实验课上,甲组同学运用下列实验方法探究碱的性质.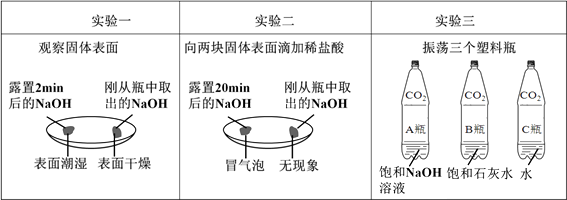
①由上图实验一可知,氢氧化钠会吸收空气中的 , 此变化过程属于(填“物理变化”或“化学变化”).
②由上图实验二可知,氢氧化钠会吸收空气中的而变质,因此要密封保存.
②实验三中可观察到三个软塑料瓶变瘪的程度大小为A>B>C,对比A瓶与(选填“B”或“C”)瓶的实验现象可证明CO2 能与NaOH发生反应.
(二)乙组同学设计了如图所示的装置中,集气瓶内充满二氧化碳气体,瓶口的双孔塞一孔插一根连接气球的玻璃管,另一孔插一支盛有氢氧化钠溶液的胶头滴管.把胶头滴管中的氢氧化钠溶液滴入瓶中,振荡.
①实验现象: ,
反应的化学方程式为;
②小明对瓶底残留液的成分产生了兴趣,欲探究其中是否含有碳酸钠:
实验操作 | 实验现象 | 实验结论 | |
方法1 | 取样,滴加稀盐酸 | 含有碳酸钠 | |
方法2 | 取样,滴加氢氧化钙溶液 | 产生 |
小明又取样于试管中,滴加无色酚酞试液,酚酞变红,由此也得出瓶底残留液中只含有碳酸钠的结论。稍后想想又立即否定了自己的结论,理由是.