题目内容
【题目】小明用木炭粉还原氧化铜来制取铜,反应化学方程式为:______.
他根据碳的化学性质分析,认为该实验中可能会有一氧化碳产生.
【查阅资料】一氧化碳气体能使湿润的黄色氯化钯试纸变蓝色.
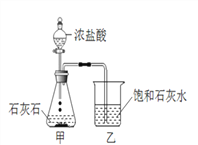
【设计实验】小明设计了下图所示的实验装置,并进行实验验证:
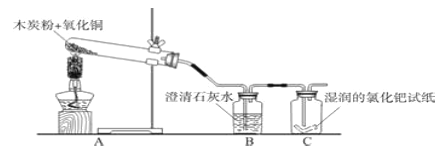
(1)A装置中酒精灯加网罩的目的是_______.
(2)刚用酒精灯给试管A加热时,B装置中就立刻产生气泡,但液体并没有浑浊的现象出现,原因是______.
(3)C中湿润黄色氯化钯试纸变蓝,说明有_____气体生成,证明小明的判断是正确的.你觉得实验产生该气体的原因可能是(写一条):______.
(4)设计装置时还要考虑环保因素,因此,要在装置C右侧导管口添加____装置.
(5)当反应结束后,小明发现一个问题:若先停止加热,______而导致试管炸裂,但若先去除B装置,则会导致________.请你帮助他设计一个实验操作,将试管中还原出的铜倒出:_________.
【答案】 C+2CuO![]() 2Cu+CO2↑ 使火焰集中,提高温度 刚加热时,试管内的空气受热膨胀从导管口逸出 CO 木炭与试管内空气中的氧气反应生成CO(或木炭与反应中生成的CO2作用生成CO 尾气处理 B装置内的石灰水会倒吸进试管中 试管中红热的铜被空气中的氧气重新氧化成氧化铜 先用弹簧夹夹紧A、B装置间的橡皮管,再熄灭酒精灯并除去B、C装置,待试管冷却后再将试管中的粉末倒出
2Cu+CO2↑ 使火焰集中,提高温度 刚加热时,试管内的空气受热膨胀从导管口逸出 CO 木炭与试管内空气中的氧气反应生成CO(或木炭与反应中生成的CO2作用生成CO 尾气处理 B装置内的石灰水会倒吸进试管中 试管中红热的铜被空气中的氧气重新氧化成氧化铜 先用弹簧夹夹紧A、B装置间的橡皮管,再熄灭酒精灯并除去B、C装置,待试管冷却后再将试管中的粉末倒出
【解析】在高温条件下碳能还原氧化铜生成铜和二氧化碳,发生的反应方程式为:C+2CuO![]() 2Cu+CO2↑;(1)A装置中酒精灯加网罩的目的是使火焰集中,提高温度;
2Cu+CO2↑;(1)A装置中酒精灯加网罩的目的是使火焰集中,提高温度;
(2)刚用酒精灯给试管A加热时,试管内的空气受热膨胀从导管口逸出,所以B装置中就立刻产生气泡,但液体并没有浑浊的现象出现;(3)一氧化碳能使湿润黄色氯化钯试纸变蓝,所以C中湿润黄色氯化钯试纸变蓝,说明有一氧化碳气体生成,产生该气体的原因可能是木炭与试管内空气中的氧气反应生成CO(或木炭与反应中生成的CO2作用生成CO); (4)一氧化碳有毒,逸出会污染空气,所以设计装置时还要考虑环保因素,因此,要在装置C右侧导管口添加尾气处理装置;(5)当反应结束后,小明发现一个问题:若先停止加热,B装置内的石灰水会倒吸进试管中而导致试管炸裂,但若先去除B装置,则会导致试管中红热的铜被空气中的氧气重新氧化成氧化铜,所以设计的实验方案:将试管中还原出的铜倒出的方法:先用弹簧夹夹紧A、B装置间的橡皮管,再熄灭酒精灯并除去B、C装置,待试管冷却后再将试管中的粉末倒出。

【题目】研究性学习小组选择“H2O2生成O2的快慢与什么因素有关”的课题进行探究,以下是他们探究的过程:
【假设】H2O2生成O2的快慢与催化剂种类有关。
【实验方案】常温下,在两瓶同质量、同浓度的H2O2溶液中,分别加入相同质量的MnO2和水泥块,测量各生成一瓶(相同体积)O2所需的时间。
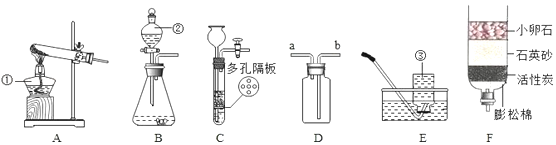
【进行实验】右下图是他们进行实验的装置图,气体发生装置中A仪器的名称是_____________,此实验中B处宜采用的气体收集方法是_______ _____。
【实验记录】
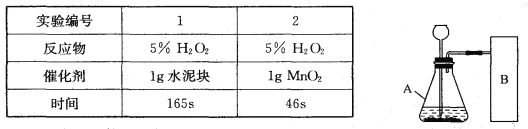
【结论】该探究过程得出的结论是_________________________。
【反思】H2O2在常温下分解缓慢,加入MnO2或水泥块后反应明显加快。若要证明MnO2和水泥块是该反应的催化剂,还需要增加实验来验证它们在化学反应前后的_____ _____是否改变。
【实验拓展】H2O2生成O2的快慢还与哪些因素有关?研究性学习小组进行了更深入的探究:
探究实验一:浓度对化学反应速率的影响
实验步骤 | 现 象 | 结 论 |
取一支试管加入3mL5%的过氧化氢溶液,然后加入少量二氧化锰。 | 缓慢有少量气泡冒出 | |
另取一支试管加入3mL15%的过氧化氢溶液,然后加入少量二氧化锰。 | 迅速有大量气泡冒出 |
请你设计:
实验用品:试管、烧杯、热水、冷水、5%过氧化氢溶液、15%过氧化氢溶液
探究实验二:温度对化学反应速率的影响
实验步骤 | 现 象 | 结 论 |
温度越高,过氧化氢分解的速率越大 |
【题目】同学们通过以下实验,探究某些酸、碱、盐之间能否发生复分解反应。
(查阅资料)BaSO4是白色固体,难溶于水,也不与盐酸反应。
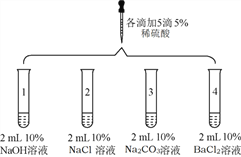
(实验一)同学们取4支试管,分别加入一定量4种溶液于试管中,再分别滴加少量的稀硫酸。
实验装置 | 实验现象 |
| 1号试管中无明显现象 |
2号试管中无明显现象 | |
3号试管中_____ | |
4号试管中有白色沉淀产生 |
(1)3号试管中的实验现象是_____。
(2)4号试管中发生复分解反应的化学方程式为_____。
(提出问题)3号、4号试管中的现象能证明硫酸与Na2CO3、BaCl2发生了复分解反应。1号、2号试管中均没有观察到明显现象,如何证明硫酸与NaOH、NaCl是否发生了复分解反应?
(实验二)同学们又进行了以下实验。
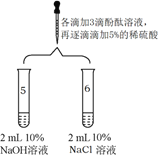
实验装置 | 实验现象 |
| 5号试管中,滴加酚酞溶液后,溶液由无色变为红色;滴加一定量稀硫酸后,溶液由红色变为无色 |
6号试管中始终无明显现象 |
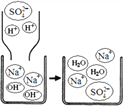
(3)5号试管中的现象能证明NaOH与稀硫酸发生了复分解反应。下图为反应的微观示意图,从微观粒子变化的角度分析,该反应的实质是_____。
(反思与评价)
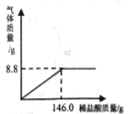
(4)同学们发现3号、4号试管中的微粒数也有变化:4号试管中的Ba2+、SO42-因生成沉淀而减少,3号试管中减少的微粒是_____。
(5)欲进一步探究2号试管中的两种物质是否发生了复分解反应,又补充了以下实验。
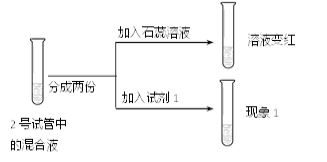
该实验证明两种物质不能发生复分解反应。请结合实验中的信息,回答下列问题:
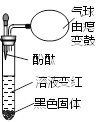
①滴加石蕊溶液的目的是_____。
②试剂1和现象1分别是_____。
(6)根据此次探究活动,你认为下列说法正确的是_____(填序号)。
A.酸、碱、盐之间并不是都能发生复分解反应
B.从微观上看,复分解反应的实质是溶液中某些离子相互结合使离子数目减少
C.判断化学反应发生,可依据有新物质生成,也可依据某一反应物消失
D.证明复分解反应没有发生,可验证某一反应物依然存在