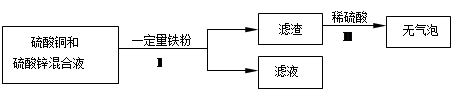题目内容
金属材料在国防建设中起着重要的作用,图1为歼-15飞机在辽宁舰上起飞.
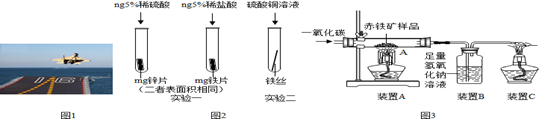
(1)铝合金用于制造飞机的外壳,铝合金材质的主要优点是_______
(2)改装前的辽宁舰舰身锈迹斑斑,钢铁的锈蚀主要是铁与空气中的_____________共同作用的结果.工业生产中常用稀盐酸除去铁制品表面的铁锈,该反应的化学方程式为___________________
(3)为了避免轮船的钢质外壳被腐蚀,通常在轮船外壳上镶嵌比铁活动性强金属.小明为探究锌、铁、铜三种金属的活动性顺序,设计了如图2的两个实验:
①实验一中,小明以“金属表面产生气泡的快慢”为标准来判断锌、铁的活动性强弱,有同学认为不够合理,理由是____________________②实验二中,若出现___________________现象,可证明铁的活动性强于铜,该反应的化学方程式为____________________
(4)辽宁舰的建造耗费了大量的钢材.某兴趣小组在实验室用图3所示装置模拟炼铁的化学原理,并测定赤铁矿中氧化铁的质量分数(装置气密性良好,反应完全且赤铁矿中的杂质不参加反应,称重赤铁矿样品的质量为wg).
①装置A中生成铁的化学方程式为__________,装置B中发生反应的化学方程式为____________.
②要测定该赤铁矿样品中氧化铁的质量分数,需要测量的数据是____________或___________.

(1)铝合金用于制造飞机的外壳,铝合金材质的主要优点是_______
(2)改装前的辽宁舰舰身锈迹斑斑,钢铁的锈蚀主要是铁与空气中的_____________共同作用的结果.工业生产中常用稀盐酸除去铁制品表面的铁锈,该反应的化学方程式为___________________
(3)为了避免轮船的钢质外壳被腐蚀,通常在轮船外壳上镶嵌比铁活动性强金属.小明为探究锌、铁、铜三种金属的活动性顺序,设计了如图2的两个实验:
①实验一中,小明以“金属表面产生气泡的快慢”为标准来判断锌、铁的活动性强弱,有同学认为不够合理,理由是____________________②实验二中,若出现___________________现象,可证明铁的活动性强于铜,该反应的化学方程式为____________________
(4)辽宁舰的建造耗费了大量的钢材.某兴趣小组在实验室用图3所示装置模拟炼铁的化学原理,并测定赤铁矿中氧化铁的质量分数(装置气密性良好,反应完全且赤铁矿中的杂质不参加反应,称重赤铁矿样品的质量为wg).
①装置A中生成铁的化学方程式为__________,装置B中发生反应的化学方程式为____________.
②要测定该赤铁矿样品中氧化铁的质量分数,需要测量的数据是____________或___________.
⑴强度大,质量轻,
(2)氧气,水,Fe2O3+6HCl═2FeCl3+3H2O,
(3)选取的酸的种类不同,铁丝表面出现红色物质,溶液由蓝色变为浅绿色,Fe+CuSO4═FeSO4+Cu,
(4)①3CO + Fe2O3 2Fe + 3CO2 2NaOH+CO2═Na2CO3+H2O,
2Fe + 3CO2 2NaOH+CO2═Na2CO3+H2O,
②反应前装置A中药品的质量,测出反应前后装置B增加的质量
(2)氧气,水,Fe2O3+6HCl═2FeCl3+3H2O,
(3)选取的酸的种类不同,铁丝表面出现红色物质,溶液由蓝色变为浅绿色,Fe+CuSO4═FeSO4+Cu,
(4)①3CO + Fe2O3
 2Fe + 3CO2 2NaOH+CO2═Na2CO3+H2O,
2Fe + 3CO2 2NaOH+CO2═Na2CO3+H2O,②反应前装置A中药品的质量,测出反应前后装置B增加的质量
试题分析:(1)合金:由一种金属跟其他一种或几种金属(或金属与非金属)一起熔合而成的具有金属特性的物质,一般说来,合金的熔点比各成分低,硬度比各成分大,抗腐蚀性能更好,铝合金材质的主要优点是:强度大,质量轻,所以用于制造飞机的外壳
(2)铁生锈的条件是:铁与O2、水接触,铁锈的主要成分:Fe2O3属于金属氧化物,可以跟酸反应,所以可以加稀盐酸除去铁制品表面的铁锈,反应的化学方程式为:Fe2O3+6HCl═2FeCl3+3H2O
(3)在利用金属与酸反应,然后通过观察产生气泡的速率来判断金属活动性时,在设计实验的时候,一定注意控制变量,而分别将相同浓度的稀盐酸和稀硫酸加入到mg的锌片和铁片中,一个是稀盐酸,另一个是稀硫酸,没有酸的种类相同这一变量,所以无法比较,所以实验设计不合理,在实验二中,由于铁的活动性比铜强,所以铁能将铜置换出来,,现象是:铁丝表面出现红色物质,溶液由蓝色变为浅绿色,化学反应方程式:Fe+CuSO4═FeSO4+Cu,
(4)①一氧化碳具有还原性,装置A中生成铁的化学方程式为;3CO + Fe2O3
 2Fe + 3CO2 ,装置A中生成的二氧化碳进入到装置B中,二氧化碳会与氢氧化钠反应,方程式为:2NaOH+CO2═Na2CO3+H2O,②赤铁矿样品中氧化铁的质量分数=氧化铁的质量/赤铁矿样品的质量×100%,所以测反应前装置A中药品的质量,即赤铁矿样品的质量,再测测出反应前后装置B增加的质量,即反应生成的二氧化碳的质量,在根据3CO + Fe2O3
2Fe + 3CO2 ,装置A中生成的二氧化碳进入到装置B中,二氧化碳会与氢氧化钠反应,方程式为:2NaOH+CO2═Na2CO3+H2O,②赤铁矿样品中氧化铁的质量分数=氧化铁的质量/赤铁矿样品的质量×100%,所以测反应前装置A中药品的质量,即赤铁矿样品的质量,再测测出反应前后装置B增加的质量,即反应生成的二氧化碳的质量,在根据3CO + Fe2O3 2Fe + 3CO2中Fe2O3和CO2的质量关系,算出Fe2O3的质量,便可求出赤铁矿样品中氧化铁的质量分数
2Fe + 3CO2中Fe2O3和CO2的质量关系,算出Fe2O3的质量,便可求出赤铁矿样品中氧化铁的质量分数
练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目

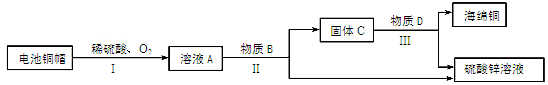
 2CuSO4+2H2O
2CuSO4+2H2O