题目内容
【题目】如图表示的是一些物质在常温下的近似pH,回答下列问题:

(1)在少量厨房清洁剂中滴入几滴酚酞,溶液呈_________色;
(2)酸雨的酸性比正常雨水的酸性_________(填“强”或“弱”);
(3)食醋是家庭厨房中常备的一种酸性调味品,在常温下,溶质质量分数为3%的食醋的pH_________(填“大于”或“小于”4%的食醋的pH,要使食醋的pH升高,可采用的方法是_____________。
(4)测量苹果汁pH时,pH试纸是否需要先用蒸馏水润湿_________(填“是”或“否”)。
【答案】红 强 大于 加水稀释 否
【解析】
(1)厨房清洁剂的pH在12~13之间,大于7,显碱性,酚酞溶液遇碱性溶液变红色,故在少量厨房清洁剂中滴入几滴酚酞,溶液呈红色。
(2)根据题意,酸雨的pH在4~5之间,正常雨水的pH在5~6之间,酸雨的pH小于正常雨水的pH,故酸雨的酸性比正常雨水的强。
(3)酸性溶液溶质质量分数越大酸性越强,所以减低酸性应对溶液进行稀释,由于酸的pH值是越大酸性越弱,所以3%的食醋的pH大于4%的食醋的pH,要使食醋的pH升高,可采用的方法是加水稀释。
(4)测量苹果汁pH时,pH试纸不需要先用蒸馏水润湿,否则测得的pH偏大。

 优加精卷系列答案
优加精卷系列答案【题目】氢氧化钠和氢氧化钙是两种常见的碱,化学实验活动课上,同学们进行了如图所示的实验。

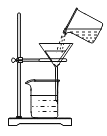
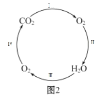
(1)实验一中,B试管中发生反应的化学方程式为________________。A、B两支试管中共同的实验现象是___________________,其原因是_________________。
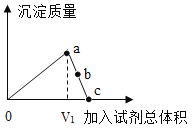
(2)实验二中,观察到C中有白色沉淀生成,该白色沉淀是___________(填化学式)。
①D试管中无现象,为了探究二氧化碳是否与氢氧化钠反应,甲同学又设计了如图所示的对比实验:

小洪同学认为该实验设计不符合对比实验的基本原则。理由是____________________。
②为了探究D中反应后的溶液中是否有碳酸钠,乙同学进行了如下探究:
方案 | 实验步骤 | 实验现象 | 结论、反应的化学方程式 |
一 | 取少量反应后溶液于一支试管中,加入过量的稀盐酸 | _______________________ | _________________________ |
二 | 取少量反应后溶液于另一支试管中,_________________ | ______________________ | 有碳酸钠生成:____________________ |
③丙同学设计下列实验来证明反应后的溶液中,除生成物碳酸钠还有剩余的氢氧化钠。
实验操作 | 实验现象 | 实验结论 |
取D中少量溶液于另一试管中,加入适量的 | 产生白色沉淀,酚酞试液变红 | 溶液中还有氢氧化钠存在 |
小军评价实验操作③的结论不正确,理由是___________________。