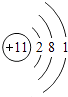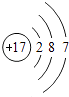题目内容
【题目】下面是元素周期表中某些元素的部分信息,请回答下列问题:
第3周期 | 11 Na | 镁 | … | 16 S | 17 Cl | 18 Ar |
第4周期 | 19 K | 20 Ca | … | |||
(1)Mg元素的核电荷数= .
(2)钠元素和硫元素处于同一周期的原因是 .
(3)钠元素和钾元素的化学性质相似的原因是 .
(4)请写出钾元素和硫元素形成的化合物的化学式 .
【答案】
(1)12
(2)其核外电子层数相同
(3)最外层电子数相同
(4)K2S
【解析】解:(1)因为同一周期的元素电子层数相等,且从左向右核电荷数依次增大1,所以由钠的核电荷数是11,可知镁的核电荷数为12;(2)因为同一周期的元素电子层数相等,所以钠元素和硫元素处于同一周期的原因是其核外电子层数相同;(3)因为元素的最外层电子数决定元素的性质,由表中数据可知钠元素和钾元素的最外层电子数相等,所以两者化学性质一定相似;(4)由表中数据可知钾元素最外层电子数是1,易失掉该电子,所以其化合价常表现为+1价,而硫原子最外层电子数6,易得到两个电子,所以其化合价常表现为﹣2价,所以两者形成的化合物化学是为:K2S;
所以答案是:(1)12;(2)其核外电子层数相同;(3)最外层电子数相等;(4)K2S;

【题目】课外活动小组的同学在测定由NaCl和Na2CO3形成的固体混合物组成时,进行了以下实验:取40 g固体混合物配成溶液,平均分为四份,然后分别加入一定质量分数的CaCl2溶液,实验数据见下表:
实验一 | 实验二 | 实验三 | 实验四 | |
原固体混合物质量 | 10g | 10g | 10g | 10g |
加入CaCl2溶液质量 | 10g | 20g | 30g | 40g |
生成的沉淀的质量 | 2g | m | 5g | 5g |
请分析表中数据回答并计算[(4)要求写计算过程]
(1)生成的沉淀是(填写化学式)
(2)10g原固体混合物配成的溶液和足量CaCl2溶液反应,最多生成沉淀质量为g.
(3)m=g.
(4)原固体混合物中Na2CO3的质量分数是多少?