题目内容
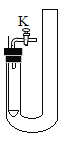
【题目】利用下图装置进行实验。
实验装置 | 实验1 探究燃烧的条件 | 实验2制取二氧化碳 |
| Ⅰ.燃烧匙中放置一小块白磷(着火点为40℃),装置中盛放80℃的热水(浸没白磷)。 Ⅱ.打开K,从导管口鼓入空气至白磷露出水面,关闭K。 | Ⅰ.燃烧匙中盛有大理石,装置中盛放一定量的稀盐酸(浸没大理石)。 Ⅱ.打开K,收集二氧化碳。Ⅲ.…… |
(1)实验1中,能证明燃烧需要与氧气接触的实验现象是 ____________________;
(2)实验2中,制取二氧化碳的化学方程式为___________________;
(3)实验2中,为使反应停止,Ⅲ中的操作是____________________________。
【答案】白磷露出水面前不燃烧,露出水面时开始燃烧 CaCO3+2HCl=CaCl2+H2O+CO2↑ 关闭K,左侧玻璃管中液体被压至燃烧匙以下,反应停止
【解析】
(1)燃烧匙中放置一小块白磷(着火点为40℃),装置中盛放80℃的热水(浸没白磷),此时白磷没有燃烧,因为热水中不含氧气。实验1中,打开K,从导管口鼓入空气至白磷露出水面,白磷和氧气接触,会燃烧生成大量白烟,证明燃烧需要氧气;故答案为:白磷露出水面前不燃烧,露出水面时开始燃烧;
(2)实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙、水和二氧化碳,配平即可;故答案为:CaCO3+2HCl=CaCl2+H2O+CO2↑;
(3)实验2中,关闭K,左侧玻璃管中有二氧化碳生成,气压增大,当液体被压至燃烧匙以下,大理石和稀盐酸实现固液分离,反应停止;故答案为:关闭K,左侧玻璃管中液体被压至燃烧匙以下,反应停止。

【题目】某化学兴趣小组为探究化学反应中的能量变化,进行以下实验:
(探究一)盐酸与氢氧化钠的反应
(1)写出氢氧化钠溶液与盐酸反应的化学方程式:_________________________________。
(2)甲同学设计实验:向一定量氢氧化钠固体中倒入20mL 4%盐酸,用温度计测量反应前后各溶液的温度。乙同学认为该实验方案不合理,其理由是_________________________。
(3)丙同学设计了如下三组实验,请你帮助他完成实验方案:
实验编号 | 实验方案 |
实验1 | 向20mL 4%盐酸中倒入20mL水,测定稀释前后溶液的温度。 |
实验2 | 向20mL 5%氢氧化钠溶液中________________,测定稀释前后溶液的温度。 |
实验3 | _______________________________________________________________。 |
(4)丙同学观察到的实验现象是:实验3溶液升高的温度远大于实验1与实验2溶液升高的温度之和,由此你能得出的实验结论是①____________;②____________。
(探究二)盐酸与碳酸氢钠溶液的反应。
下图是丁同学在20℃、基本隔热条件下利用温度传感器,分别测定向20mL水和20mL饱和碳酸氢钠溶液中各倒入20mL 13.7%盐酸的温度与时间变化曲线。
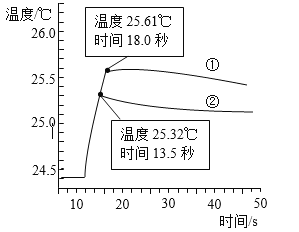
曲线①为水+13.7%盐酸温度变化曲线
曲线②为饱和碳酸氢钠溶液+13.7%盐酸温度变化曲线
实验测得饱和碳酸氢钠溶液稀释时温度变化不大,可忽略不计,据此回答下列问题:
(5)18.0秒后,曲线①逐渐下降的原因是____________________________________;
(6)比较曲线①和曲线②,你认为13.7%盐酸与饱和碳酸氢钠溶液的反应是________(填“放热”或“吸热”)反应,其理由是_________________________。
【题目】下列图象一定不能正确反映其对应关系的是( )
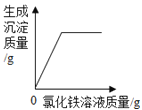
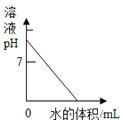
|
|
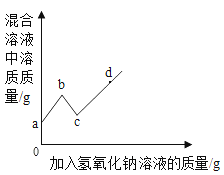
|
|
A.某温度下,向一定量的氯化钠溶液中不断加入水 | B.向一定量的氢氧化钠和氯化钠的混合溶液中逐滴加入氯化铁溶液 | C.向一定量的氢氧化钠溶液中逐滴加水稀释 | D.向两个分别盛有质量相等的氢氧化镁和氧化镁固体的烧杯中,逐滴加入溶质质量分数相同的稀盐酸 |