题目内容
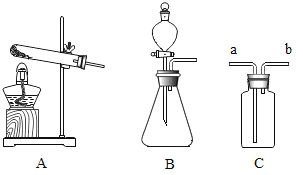
【题目】下列装置常用于实验室制取气体.
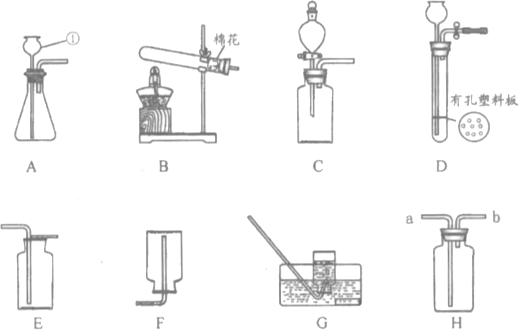
(1)写出上图中指定仪器的名称:①______________。
(2)用高锰酸钾制取并收集纯度相对较大的氧气,可以选择的装置是________(填字母)。该反应的化学方程式为____________________________,属于________(填基本反应类型)反应。
(3)制取二氧化碳时,如需控制产生气体的速率,发生装置最好选用____________(填字母),使用装置H进行排空气法收集二氧化碳,气体应从________(选填“a”或“b”)端通入。
(4)实验室制取硫化氢气体的原理:室温下,块状不溶性的硫化亚铁(FeS)固体与稀硫酸反应(另一产物为硫酸亚铁)。
①写出该反应的化学方程式:___________________。
②若想控制反应的发生和停止,可选用的发生装置为______________(填字母)。
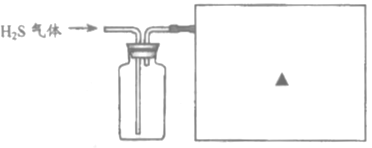
③已知硫化氢气体有毒,密度比空气大,能溶于水且易与NaOH溶液反应。请在下图方框内补充完整收集硫化氢气体的装置图。_______
【答案】长颈漏斗 BG 2KMnO4![]() K2MnO4+MnO2+O2↑ 分解 C a FeS+H2SO4=FeSO4+H2S↑ D
K2MnO4+MnO2+O2↑ 分解 C a FeS+H2SO4=FeSO4+H2S↑ D 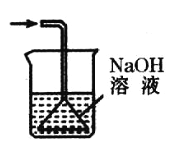
【解析】
(1)仪器①的名称是长颈漏斗,故填长颈漏斗。
(2)用高锰酸钾制取氧气是加热固体制取气体,发生装置应选用固体受热装置,选择B,收集纯度相对较大的氧气应选择排水法收集,选择G,故填BG;
高锰酸钾受热反应生成锰酸钾、二氧化碳和氧气,故反应的化学方程式写为:2KMnO4![]() K2MnO4+MnO2+O2↑;
K2MnO4+MnO2+O2↑;
由化学方程式可知,该反应是一种物质反应生成三种物质,属于分解反应,故填分解。
(3)制取二氧化碳时,如需控制产生气体的速率,发生装置选择带有分液漏斗的固液常温发生装置,故填C;
二氧化碳的密度大于空气的密度,气体应从长管进入瓶中,故填a。
(4)①硫化亚铁与稀硫酸反应生成硫酸亚铁和硫化氢气体,故反应的化学方程式写为:FeS+H2SO4=FeSO4+H2S↑。
②控制反应的发生和停止,应选择带有有孔塑料板的固液常温发生装置,故填D。
③硫化氢气体能溶于水,用氢氧化钠溶液吸收硫化氢气体时,应在导管口加装倒扣的漏斗防止液体倒吸,故填 。
。

 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案【题目】实验室常用加热氯酸钾与二氧化锰混合物的方法制取氧气,写出反应的化学方程式:______。
小芳发现,氯酸钾与氧化铜混合加热,也能较快产生氧气,于是进行如下探究:
(提出猜想)除MnO2外、CuO也可以作KClO3分解的催化剂。
(完成实验)按下表进行实验:测定分解温度(分解温度越低,催化效果越好(℃)
实验编号 | 实验药品 | 分解温度(℃) |
① | KClO3 | 580 |
② | KClO3、MnO2(质量比1:1) | 350 |
③ | KClO3、CuO(质量比1:1) | 370 |
④ | KClO3、MnO2(质量比1:3) | 320 |
(分析数据、得出结论)
(1)由实验______的对比,证明猜想合理:
(2)对比实验①②④你得出的认识是______。
(反思)
(1)若要证明CuO是该反应的催化剂,还要验证它在化学反应前后质量和______不变;
(2)同种催化剂,颗粒大小可能影响催化效果,请设计实验方案进行验证______。