题目内容
铝作为食品污染源之一,成人每日摄入量应控制在4mg以下,炸油条时需加入明矾晶体作为膨松剂.已知明矾晶体的化学式为KAl(SO4)2?12H2O,相对分子质量为474.
(1)计算明矾晶体中铝元素的质量分数;
(2)在1kg炸成的油条中,含有明矾晶体2g,试通过计算说明成人每日食用100g油条,铝元素是否超过安全摄入量?
(1)计算明矾晶体中铝元素的质量分数;
(2)在1kg炸成的油条中,含有明矾晶体2g,试通过计算说明成人每日食用100g油条,铝元素是否超过安全摄入量?
考点:元素的质量分数计算,化合物中某元素的质量计算
专题:化学式的计算
分析:(1)根据物质中某元素的质量分数=
×100%,进行解答;
(2)根据物质中某元素的质量=该物质的质量×该元素的质量分数,进行解答.
| 该元素的相对原子量×原子个数 |
| 该物质的相对分子质量 |
(2)根据物质中某元素的质量=该物质的质量×该元素的质量分数,进行解答.
解答:解:(1)根据物质中某元素的质量分数═
×100%,可得明矾晶体中铝元素的质量分数=
×100%=5.7%;
(2)成人每日食用100g油条含有铝元素的质量为:
(2×5.7%×
)×1000 mg=11.4mg;
11.4mg>4mg 超过安全标准;
答:矾晶体中铝元素的质量分数为5.7%;成人每日食用100g油条,铝元素超过安全摄入量.
| 该元素的相对原子量×原子个数 |
| 该物质的相对分子质量 |
| 27 |
| 39+27+(32+16×4)×2+12×(1×2+16) |
(2)成人每日食用100g油条含有铝元素的质量为:
(2×5.7%×
| 100 |
| 1000 |
11.4mg>4mg 超过安全标准;
答:矾晶体中铝元素的质量分数为5.7%;成人每日食用100g油条,铝元素超过安全摄入量.
点评:本题主要考查化学式的意义、根据化学式确定组成物质元素之间的质量关系进行解题的能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列各变化能用如图所示图象表示的是( )
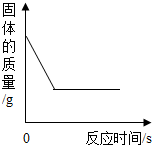

| A、加热一定质量的高锰酸钾固体 |
| B、向一根锈铁钉中加入足量稀盐酸 |
| C、向一定量的铁粉中加入足量硫酸铜溶液 |
| D、向一定量的锌铜合金中加入足量的稀硫酸 |