题目内容
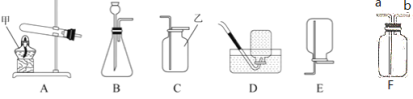
【题目】请结合下列实验常用装置,回答有关问题。
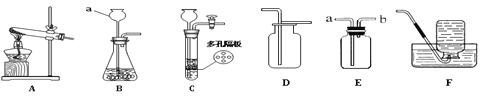
(1)实验室用氯酸钾制取氧气的反应方程式为_________________,
(2)可选用的发生装置和收集装置的组合是_________________。
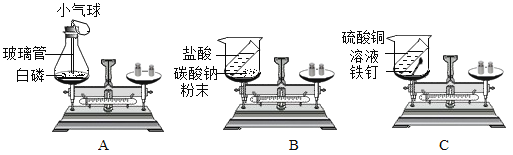
(3)乙炔(C2H2)是无色、无味、易燃的气体,乙炔的密度比空气略小,难溶于水。乙炔由碳化钙(块状固体)与水反应生成,同时生成一种白色固体。已知碳化钙与水反应非常剧烈。实验室欲制取并收集纯净的乙炔,若选择的装置C,其优点是___________。
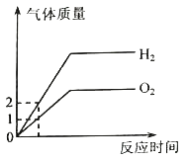
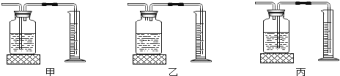
(4)如果用E装置来测定氧气的体积(氧气从装置左端进入),应选用下图中的________(填编号)装置。
【答案】2KClO3![]() 2KCl+3O2↑ AD 或AE或AF 可以控制反应的发生与停止 丙
2KCl+3O2↑ AD 或AE或AF 可以控制反应的发生与停止 丙
【解析】
(1)氯酸钾在二氧化锰做催化剂的条件下加热生成氯化钾和氧气,反应的方程式为:2KClO3![]() 2KCl+3O2↑
2KCl+3O2↑
(2)氯酸钾制取氧气的装置属于固固加热型装置,故发生装置选A。氧气难溶于水,密度比空气的密度大,故收集装置选D或E或F。故组合装置为AD 或AE或AF。
(3)装置C中利用了隔板将药品放在隔板上面,可以控制反应的发生与停止。
(4)该装置测定氧气的原理是多功能瓶中收集氧气,将水排入量筒中,收集到多少体积的氧气,就有多少体积的水排到量筒中,故气体由短管通入,水由长管排出,故选丙。

练习册系列答案
相关题目