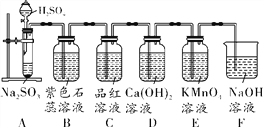
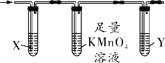
题目内容
【题目】某同学通过氯酸钾制取氧气,相关数据如表:
反应前物质的总质量/g | 反应后剩余物的总质量/g |
25 | 15.4 |
请计算:
(1)该同学制得氧气的质量为g。
(2)参加反应的氯酸钾的质量。
【答案】
(1)9.6g
(2)24.5g
【解析】(1)氯酸钾分解生成氯化钾和氧气,氧气是气体,会逸散到空气中。根据质量守恒定律化学反应前后物质的总质量不变,故减少的质量即为生成的氧气的质量。氧气的质量=25g-15.4g=9.6g;(2)利用化学方程式,根据氯酸钾和氧气反应的质量比即可计算出参加反应的氯酸钾的质量。
设参加反应的氯酸钾的质量为x;
2KClO3 | 3O2↑ |
245 | 96 |
x | 9.6g |
![]() x=24.5g
x=24.5g
答:该同学制得氧气的质量为9.6g,参加反应的氯酸钾的质量为24.5g。
利用质量守恒定律可以得出氧气的质量,依据氧气的质量结合方程式可以计算出氯酸钾的质量

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目