题目内容
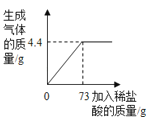
【题目】某化学兴趣小组欲测定谋铁粉混合物中铁的质量分数,他们进行了如右图所示的实验。请计算:

(1)混合物中铁的质量;
(2)反应后烧杯中稀硫酸无剩余,请计算所用稀硫酸中溶质的质量分数;
(3)欲用98%的浓硫酸配制该浓度的稀硫酸200g需要水多少克?
【答案】(1)5.6g (2)19.6%; (3)160g
【解析】
试题分析:(1)由图可知,滤渣4.4g为碳,故铁的质量为10g-4.4g=5.6g
(2)设该稀硫酸中溶质的质量为x
Fe + H2SO4 = FeSO4 + H2↑
56 98
5.6g x
56/5.6g=98/x
x=9.8g
稀硫酸中溶质的质量分数为9.8g/50g×100%=19.6%
(3)设需要浓硫酸的质量为y,则
98%× y=200g×19.6%
y=40g
需要水的质量:200g―40g=160g

练习册系列答案
相关题目