题目内容
【题目】水和溶液对于人类的生产和生命活动有重大的意义。
(1)生活中可以用_____区分硬水和软水,通过_____的方法将硬水软化。
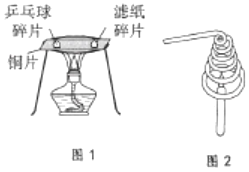
(2)电解水的实验中,正负两级产生的气体体积比为_____,电解水的反应的化学方程式是_____,通过实验可以得出水是由_____组成的。
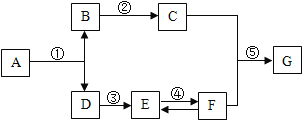
(3)用氯化钠固体和水配制6%的氯化钠溶液50g,则需要氯化钠_____g,量筒需要选择_____mL的(选10mL,50mL,100mL,500mL)。如图正确的操作顺序是_____(填字母序号),若量取水时仰视读数,其他操作均正确,则配制的氯化钠溶液中溶质质量分数_____6%(填“>”“<”或“=”)。

【答案】肥皂水 煮沸 1:2 2H2O![]() 2H2↑+O2↑ 氢元素和氧元素(或氢氧元素或H和O) 3 50 BCAED <
2H2↑+O2↑ 氢元素和氧元素(或氢氧元素或H和O) 3 50 BCAED <
【解析】
根据化学实验基础仪器的使用、操作及注意事项分析解答;根据电解水的化学反应原理分析解答。
(1)由于肥皂水和硬水中所含的钙离子或者镁离子反应生成沉淀,所以生活中可以用肥皂水区分硬水和软水;由于加热煮沸可以使可溶性钙镁离子转化为难溶性的碳酸钙和氢氧化镁,所以生成中常用煮沸的方法将硬水软化。
(2)电解水的实验中,熟记对应的现象为“正氧负氢,氢二氧一”。所以正负两极产生气体的体积比为 1:2,电解水的反应的化学方程式是:2H2O![]() 2H2↑+O2↑,由于水为纯净物,而生成的氢气和氧气均为纯净物吗,且是氢元素和氧元素组成的,所以根据质量守恒定律可以通过实验可以得出水是由氢元素和氧元素(或氢氧元素或H和O)组成的。
2H2↑+O2↑,由于水为纯净物,而生成的氢气和氧气均为纯净物吗,且是氢元素和氧元素组成的,所以根据质量守恒定律可以通过实验可以得出水是由氢元素和氧元素(或氢氧元素或H和O)组成的。
(3)用氯化钠固体和水配制6%的氯化钠溶液50g,则需要氯化钠=50g×6%=3g,需要水的质量为50g﹣3g=49g,合47mL,量筒需要选择50mL的;
用氯化钠固体和水配制6%的氯化钠溶液。先计算需要的氯化钠的质量和水的质量(水的质量折合为体积),然后称取固体量取液体,混合,搅匀。给出的图中线打开盛有氯化钠的试剂瓶取出氯化钠进行称量固体,然后将固体倒入烧杯中,加入水进行搅拌,所以正确的操作顺序是 BCAED.若量取水时仰视读数,其它操作均正确,由于仰视读数偏小,实际液体多了,所以导致配制的氯化钠溶液中溶质质量分数<6%。
故答案为:(1)肥皂水;煮沸;(2)1:2; 2H2O![]() 2H2↑+O2↑,氢元素和氧元素或氢氧元素或H和O);(3)3;50;BCAED;<。
2H2↑+O2↑,氢元素和氧元素或氢氧元素或H和O);(3)3;50;BCAED;<。

 快乐暑假暑假能力自测中西书局系列答案
快乐暑假暑假能力自测中西书局系列答案【题目】生铁是铁和碳等元素形成的合金![]() 为测定某生铁样品中铁的质量分数所进行的某次实验中,称取粉碎后的该生铁样品
为测定某生铁样品中铁的质量分数所进行的某次实验中,称取粉碎后的该生铁样品![]() ,放入烧杯中,向其中加入
,放入烧杯中,向其中加入![]() 的稀硫酸,充分搅拌使其恰好完全反应
的稀硫酸,充分搅拌使其恰好完全反应![]() 碳等杂质既不溶于水也不与酸反应
碳等杂质既不溶于水也不与酸反应![]() 测得的实验数据如下:
测得的实验数据如下:
反应前 | 反应后 | |
烧杯及其中物质的总质量 |
|
|
根据实验数据进行计算![]() 结果保留一位小数
结果保留一位小数![]() :
:
![]() 产生氢气的质量为______g;
产生氢气的质量为______g;
![]() 该生铁样品中铁的质量分数_______;
该生铁样品中铁的质量分数_______;
![]() 反应后所得溶液的溶质质量分数_______.
反应后所得溶液的溶质质量分数_______.