题目内容
在一次探究活动中,小强用塑料吸管向新制的澄清石灰水中不断吹气,在吹气的过程中发现石灰水先出现浑浊后又变澄清,他感到很意外。小强又将纯净的CO2持续通入新制的澄清石 灰水中,一段时间后,观察到的现象与上次相同。
灰水中,一段时间后,观察到的现象与上次相同。
(1)小强做第二次实验的目的是 ▲ 。
(2)小强从老师那里得知:CO2能与CaCO3和H2O继续反应生成Ca(HCO3)2。由此
小强推测出Ca(HCO3)2的一条物理性质是 ▲ 。
(3)已知实验老师配置新制的澄清石灰水时是用生石灰配制而成,请写出该反应的化学方程式 ▲ 。工业上所用的生石灰是由石灰石煅烧而成(已知:CaCO3 CaO+CO2↑)。如果煅烧含杂质10%的石灰石100 t(杂质不参与反应),可制得含氧化钙80%的生石灰的质量是多少?(写出计算过程)
CaO+CO2↑)。如果煅烧含杂质10%的石灰石100 t(杂质不参与反应),可制得含氧化钙80%的生石灰的质量是多少?(写出计算过程)
(1)排除呼出气体中其它气体产生的干扰 (2)易溶于水
(3)CaO+H2O ====Ca(OH)2
解:设可制得含CaO80%的生石灰质量为x
CaCO3  CaO+CO2↑
CaO+CO2↑
100 56
100t×(1-10%) x×80 %
%
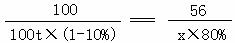
解得: x=63t
答:略。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
 23、①一双善于发现问题的眼睛能够带来许多意想不到的知识.
23、①一双善于发现问题的眼睛能够带来许多意想不到的知识.