题目内容
【题目】同学们在学习了焦炭还原氧化铁的反应后,联想到单质碳的一些化学性质,对反应后的气体成份产生了疑问,并对其气体成份进行了如下探究。
(猜想)①气体产物全部是![]() ;
;
②气体产物全部是______。
③气体产物是CO和![]() 的混合物
的混合物
(查阅资料)CO气体能使湿润的黄色氯化钯试纸变蓝色。
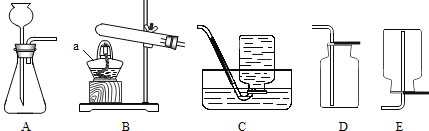
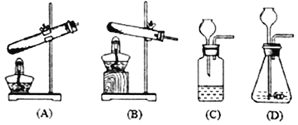
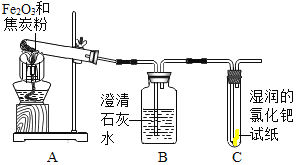
(设计实验)根据各自的猜想,他们共同设计了如图的实验装置进行探究。
(现象与分析)
预期的现象 | 相应的结论 |
如果装置B中澄清石灰水变浑浊,装置C无明显现象; | 则猜想①成立 |
如果装置B中澄清石灰水变无明显变化,装置C ______ 。 | 则猜想 ______ 成立 |
如果装置B ______ ,装置C ______ | 则猜想 ______ 成立。 |
(结论)根据实验结果猜想③成立,同学们的疑问是合理的。
(反思)
![]() 同学们对CO产生的原因进行了首先
同学们对CO产生的原因进行了首先![]() 与焦炭反应,生成的其中一种产物和焦炭又发生了化学反应,产生了CO;请你用化学方程式表示生成CO的原因______,______。
与焦炭反应,生成的其中一种产物和焦炭又发生了化学反应,产生了CO;请你用化学方程式表示生成CO的原因______,______。
![]() 根据上述实验,可以得出焦炭具有______性。
根据上述实验,可以得出焦炭具有______性。
【答案】CO 湿润的黄色氯化钯试纸变蓝色 ② 澄清石灰水变浑浊 湿润的黄色氯化钯试纸变蓝色 ③ C+ 2Fe2O3 ![]() 4Fe + 3CO2↑ C + CO2
4Fe + 3CO2↑ C + CO2 ![]() 2CO 还原
2CO 还原
【解析】
猜想:
根据质量守恒定律可知,木炭粉与氧化铁反应生成物有三种可能:①气体产物全部是CO2②气体产物全部是CO③气体产物是CO2和CO的混合物;
现象与
如果装置B中澄清石灰水变无明显变化,装置C湿润的黄色氯化钯试纸变蓝色,说明气体是一氧化碳;
如果装置B中澄清石灰水变浑浊,装置C中湿润的黄色氯化钯试纸变蓝色,说明气体中含有二氧化碳和一氧化碳,实验过程如下所示:
预期的现象 | 相应的结论 |
如果装置B中澄清石灰水变浑浊,装置C无明显现象; | 则猜想①成立 |
如果装置B中澄清石灰水变无明显变化,装置C湿润的黄色氯化钯试纸变蓝色。 | 则猜想②成立 |
如果装置B中澄清石灰水变浑浊,装置C中湿润的黄色氯化钯试纸变蓝色。 | 则猜想③成立。 |
反思:
![]() 高温条件下,氧化铁和碳反应生成铁和二氧化碳,二氧化碳和碳反应生成一氧化碳,反应的化学方程式为:C+ 2Fe2O3
高温条件下,氧化铁和碳反应生成铁和二氧化碳,二氧化碳和碳反应生成一氧化碳,反应的化学方程式为:C+ 2Fe2O3 ![]() 4Fe + 3CO2↑,C + CO2
4Fe + 3CO2↑,C + CO2 ![]() 2CO
2CO
![]() 根据上述实验,可以得出焦炭具有还原性。
根据上述实验,可以得出焦炭具有还原性。