��Ŀ����
����Ŀ����ͼ��ʾΪʵ�����г��������Ʊ�������������ռ��ͽ���ʵ��̽���IJ�����������װʵ��װ��ʱ�����ظ�ѡ����������ij��ѧС���ͬѧ��������������и�ʵ�顣
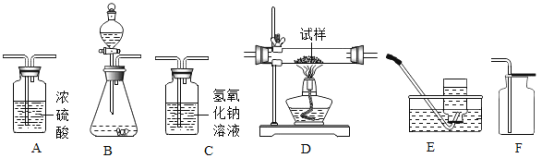
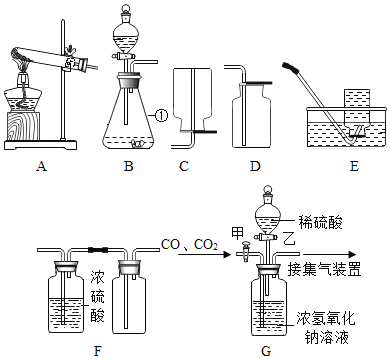
��1���Թ���������ҺΪԭ�ϣ���������������������ʵ��������ȡ���ռ����������������Ҫ�����ʵ��װ�ã����������������װ�õ������ԡ�
����ѡװ�õ�����˳��Ϊ_____����������дװ�������ĸ����
����ȡ������������Ӧ�Ļ�ѧ����ʽΪ_____��
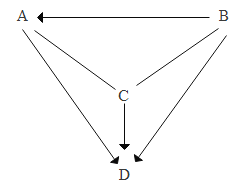
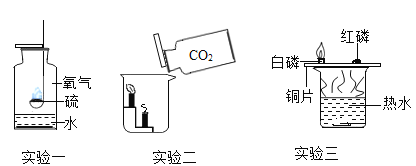
�����й���������ȡ�����ʵ������У�����ȷ����_____���A����B����C����D��֮һ����
A ʵ����������ʱ��Ӧ�ȼ���ҩƷ���ټ��װ�õ�������
B �ڴ˷�Ӧǰ�������̵������ͻ�ѧ���ʶ��������ı�
C ��˿�ڴ����о���ȼ��ʱ���������䣬���ɺ�ɫ����
D ������һ�ֻ�ѧ���ʱȽϻ��õ�����
��2���ø��﴿������������ά�ص���ɽ��з���̽��ʵ�飨������ʾ��ά��ֻ��C��H��O����Ԫ�أ�����ѡװ�ð��������D��A��C����ʯ�Ҹ���ܡ���˳�����ӣ�ʵ��ǰ���װ�õ������ԣ������������Ļ�ѧ��Ӧ����ȫ��ֽ��У���װ��D�IJ������з�����ά������������Ϊwg����ַ�Ӧ���װ��A����������ag��װ��C����������bg������ά����̼Ԫ�ص���������Ϊ_____���������ú���ĸ�Ĵ���ʽ��ʾ����
��ʵ����ʹ�õ�����δ����������������ά���е�̼Ԫ������Ԫ�ص���������ʵ��ֵ�ȽϽ�_____���ƫ��ƫС��������һ�¡�����ȷ����֮һ����
��3����һ����̼���壨��������������̼��ˮ�������ⶨij���������FexOy��������Ԫ����ɱ�������ѡװ�ð�����������A1��D��C��A2����˳�����ӣ�A1��A2ΪŨ����ϴ��ƿ��ʵ��ǰ����װ�������ԣ������������Ļ�ѧ��Ӧ����ַ�Ӧ��������ʵ�鲢��¼ʵ�����ݣ������ʾ��
װ�ñ�� | A1��Ũ���� | D�в������ڹ��� | C����Һ |
��Ӧǰ���� | 150g | 14.4g | 200g |
��Ӧ������ | 152.7g | 11.2g | 213.2g |
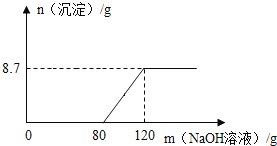
����ѡ��������ݼ���FexOy��x��y=_____����д��������ȣ���
�ڴӻ����Ƕȿ��ǣ���ʵ�鷽����ƻ����ڲ�����֮������ľ���Ľ�������_____��
���𰸡�BAF 2H2O2![]() 2H2O+O2�� A
2H2O+O2�� A ![]() ƫС 1��1 A2װ�ú�����β������װ��
ƫС 1��1 A2װ�ú�����β������װ��
��������
��1����ʵ�����ù���������Һ��ȡ������ѡ��װ��B������װ�ã���Ũ�������������ѡ��װ��A������װ�ã��������ܶȱȿ������������ſ�������ѡ��װ��F���ռ�װ�ã�����ѡװ�õ�����˳��ΪBAF��
���ù���������ȡ����ʱ����������Ϊ��������Ӧ�Ļ�ѧ����ʽΪ2H2O2![]() 2H2O+O2����
2H2O+O2����
��A��ʵ����������ʱ��Ӧ�ȼ��װ�õ������ԣ��ټ���ҩƷ����A����
B���ڴ˷�Ӧǰ�����������ͻ�ѧ���ʶ��������ı䣬���������Ǹ÷�Ӧ�Ĵ�������B��ȷ��
C����˿�ڴ����о���ȼ��ʱ���������䣬���ɺ�ɫ���壬��C��ȷ��
D��������һ�ֻ�ѧ���ʱȽϻ��õ����壬��D��ȷ����ѡA��
��2��װ��C���ӵ�����Ϊ���ɶ�����̼�����������������غ㶨�ɣ��ɵö�����̼��̼Ԫ�ص�������������ά����̼Ԫ�ص�����������wg��ά����̼Ԫ�ص�����Ϊ![]() ������wg��ά����̼Ԫ�ص���������Ϊ
������wg��ά����̼Ԫ�ص���������Ϊ![]() ����ʵ��������δ�������ˮ������ƫ��������ά������Ԫ�ص�����ƫ�����Բ��������ά���е�̼Ԫ������Ԫ�ص���������ʵ��ֵ�ȽϽ�ƫС��
����ʵ��������δ�������ˮ������ƫ��������ά������Ԫ�ص�����ƫ�����Բ��������ά���е�̼Ԫ������Ԫ�ص���������ʵ��ֵ�ȽϽ�ƫС��
��3����һ����̼��ԭ����������������ڼ��ٵ�������Ϊ����������Ԫ�ص�������ʣ����������Ϊ������������������D�в����ܵ����ݿ�֪������������Ԫ�ص�����Ϊ11.2g����Ԫ�ص�����Ϊ14.4g��11.2g=3.2g����������FexOy����Ԫ������Ԫ�ص��������г�ʽ��Ϊ��![]() �����x��y =1��1����C����Һ���ӵ��������˷�Ӧ���ɶ�����̼��������������ԭһ����̼�����ж�����̼�����������ݲ���������������x��y�ı�ֵ��
�����x��y =1��1����C����Һ���ӵ��������˷�Ӧ���ɶ�����̼��������������ԭһ����̼�����ж�����̼�����������ݲ���������������x��y�ı�ֵ��
�ڷ�Ӧ��Ϊһ����̼��һ����̼�ж�������Ҫ��A2װ�ú��β������װ�á�

 ������Ӧ�������������ϵ�д�
������Ӧ�������������ϵ�д� �㽭֮�ǿ�ʱ�Ż���ҵϵ�д�
�㽭֮�ǿ�ʱ�Ż���ҵϵ�д�