题目内容
【题目】(1)黑火药是我国古代四大发明之一,黑火药爆炸原理可用下式表示:2KNO3 + S + 3C = X + N2 ↑+ 3CO2 ↑。请据此推出X的化学式__________。
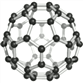
(2)C60的模型如下图所示,每个碳原子和相邻的_________个碳原子以小棍结合。若要搭建一个这样的模型,需要代表碳原子的小球_________个,需要代表化学键的连接小球的小棍__________根。
(3)已知一个SO2分子质量为nkg,一个SO3分子质量为mkg,若以硫原子质量的1/32作为相对原子质量的标准,则SO2的相对分子质量为______________。
(4)已知Fe元素在化合物里通常显+2或+3价, 因此Fe3O4可写成氧化物形式( FeO·Fe2O3)或盐的形式[Fe(FeO2)2]。Pb 在化合物里显+2价或+4价,那么Pb3O4也可以写成_____________或______________(写化学式)。
(5)一定条件下,4.8 g CH4与16.0 g O2恰好完全反应,生成10.8 g H2O、4.4 g CO2和物质X。则X的质量为_____g;该反应方程式中O2与X化学计量数之比为_______。
(6)三聚氰胺的化学式为C3H6N6,其中氮元素的质量分数为__________;常见蛋白质的含氮量相近,平均约为16%,请解释为什么不法商贩要在奶制品中添加三聚氰胺:__________________________________________。
【答案】 K2S 3 60 90 32n/(3n-2m) 2PbO·PbO2 Pb2PbO4 5.6 7:2 【答题空10】66.7% 可造成蛋白质含量偏高的假象(奶制品中蛋白质的含量是通过测定含氮量推算的)
【解析】(1)根据质量守恒定律,反应前后各种原子个数相等。反应前有2K、2N、6O、S、3C,反应后,X除外有2N、3C、6O,故X中有2K、S,化学式为K2S。(2)根据C60的模型,每个碳原子和相邻的3个碳原子以小棍结合。因为一个C60分子是由60个碳原子构成的。每个碳原子周围有3个代表化学键的连接小球的小棍,每根小棍相当于使用2次,故需要代表化学键的连接小球的小棍是3×60÷2=90根。(3)3SO2分子的质量-2SO2分子的质量= (3n-2m)kg=S原子质量,则SO2的相对分子质量为: ![]() =
=![]() 。(4)化合物中各元素化合价的代数和为零,Pb3O4也可以写成2PbO·PbO2或Pb2PbO4。(5)根据质量守恒定律,物质X的质量为:(4.8 g+16.0 g)-10.8g-4.4g=5.6g,化学方程式为:4CH4+7O2点燃2CO2+8H2O+2CO,故O2与X化学计量数之比为7:2。(6)三聚氰胺中氮元素的质量分数为:
。(4)化合物中各元素化合价的代数和为零,Pb3O4也可以写成2PbO·PbO2或Pb2PbO4。(5)根据质量守恒定律,物质X的质量为:(4.8 g+16.0 g)-10.8g-4.4g=5.6g,化学方程式为:4CH4+7O2点燃2CO2+8H2O+2CO,故O2与X化学计量数之比为7:2。(6)三聚氰胺中氮元素的质量分数为: ![]() ×100%=66.7% 。三聚氰胺中含有氮元素,添加三聚氰胺增加了氮元素的质量,可造成蛋白质含量偏高的假象。
×100%=66.7% 。三聚氰胺中含有氮元素,添加三聚氰胺增加了氮元素的质量,可造成蛋白质含量偏高的假象。