题目内容
【题目】根据实验装置图,回答下列问题:

(1)实验室用排空气法收集氧气可选用______装置(填编号)。
(2)实验室用KMnO4制氧气的反应方程式为______。用KMnO4制氧气的实验中,如果发现试管破裂,原因可能是:______(填操作失误方面的原因,指出一点即可)。
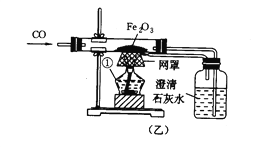
(3)实验室用B装置制取CO2的原理是______(用化学方程式表示)。可选用F装置除去CO中混有的CO2:F装置中足量澄清石灰水溶液吸收CO2反应的化学方程式为______。
(4)实验室用无水醋酸钠固体和固体碱石灰加热制取甲烷气体。甲烷的密度比空气小,不溶于水。制取甲烷的发生、收集装置可选用______和______(填编号)。
(5)F装置可以收集和储备氢气,若用水将装置中的氢气排出,水应从______(填a或b)端通入。
【答案】 D ![]()
![]()
![]() 试管口未向下倾斜(答案合理即得分) 2HCl+CaCO3=CaCl2+H2O+CO2↑ Ca(OH)2+CO2=CaCO3↓+H2O A C(或E) a
试管口未向下倾斜(答案合理即得分) 2HCl+CaCO3=CaCl2+H2O+CO2↑ Ca(OH)2+CO2=CaCO3↓+H2O A C(或E) a
【解析】(1)氧气的密度比空气大,所以选择向上排空气法收集的装置是D;(2)高锰酸钾加热制取氧气的方程式为![]()
![]()
![]() ;据实验操作步骤及注意事项,用KMnO4制氧气的实验中,如果发现试管破裂,原因可能是未预热或受热不均匀或试管未向下倾斜;(3)实验室用B装置制取CO2的原理是:
;据实验操作步骤及注意事项,用KMnO4制氧气的实验中,如果发现试管破裂,原因可能是未预热或受热不均匀或试管未向下倾斜;(3)实验室用B装置制取CO2的原理是: ![]() ,可选用F装置除去CO中混有的CO2:F装置中足量澄清石灰水溶液吸收CO2反应的化学方程式为:
,可选用F装置除去CO中混有的CO2:F装置中足量澄清石灰水溶液吸收CO2反应的化学方程式为: ![]() ;(4)实验室用加热无水醋酸钠和碱石灰的固体混合物制取甲烷,属于“固固不加热型”,所以应选择的发生装置为 A,甲烷密度小于空气,难溶于水,可选择向下排空气法或排水法收集,所以选择收集装置为C或E;(6)因为氢气难溶于水,密度比水小,若用水将装置中的氢气排出,故水应该从长管a进入,把氢气通过短管b排出。
;(4)实验室用加热无水醋酸钠和碱石灰的固体混合物制取甲烷,属于“固固不加热型”,所以应选择的发生装置为 A,甲烷密度小于空气,难溶于水,可选择向下排空气法或排水法收集,所以选择收集装置为C或E;(6)因为氢气难溶于水,密度比水小,若用水将装置中的氢气排出,故水应该从长管a进入,把氢气通过短管b排出。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
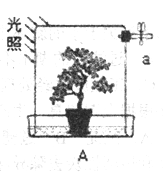
小学生10分钟应用题系列答案【题目】某课外小组的同学将玻璃罩内充满纯净的二氧化碳气体,如图A所示,在光照充足的条件下,经过一段时间后,该小组同学用注射器从a处抽取气体,测定玻璃罩内气体的成分及其含量。
【查阅资料】
①植物通过光合作用吸收二氧化碳气体,放出氧气。
②氨氧化钠和氢氧化钙(澄清石灰水)性质相似,其水溶液能与二氧化碳发生反应,且没有气体和沉淀物质生成。氧气不与氢氧化钙、氢氧化钠反应。
③二氧化碳可溶于水,一般不用排水法收集。
【实验一】检验玻璃罩内是否含有二氧化碳气体?
实验步骤 | 实验现象 | 实验结论 |
抽取适量气体,注入___________中 | 有白色沉淀产生 | ________________________ |
【实验二】采用两种方法测定玻璃罩内气体中氧气的含量。
方法1:用如图B所示的装置测量气体中氧气的含量。
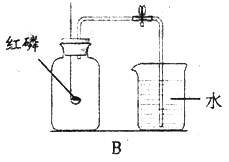
(1)将抽取出的气体用排水法收集到250mL的集气瓶中,燃烧匙中点燃红磷,反应方程式为:_______________;
(2)待装置冷却到室温后,打开弹簧夹,烧杯中的液体进入集气瓶中,其原因是________________;(2分)
(3)实验结束后,集气瓶中进入液体的体积约为150 mL。
方法2:用如图C所示的装置测量气体中氧气的含量。
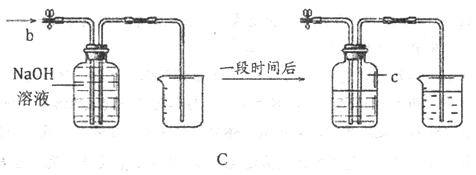
(1)抽取250mL的气体,缓缓地从b处通入装置中;
(2)实验结束后,c处气体的名称为__________,集气瓶中排出液体的体积约为125 mL。
【实验二讨论】通过对比,该小组同学发现,两种方法所得实验结果差距较大,其中实验结果更准确的是 __________(填写“方法1”或“方法2”),该方法所测得氧气约占气体总体积的________%。另一实验方法中不合理的实验操作是___________(提示:请注明是哪种方法)。
【题目】化学兴趣小组为验证质量守恒定律,做了镁条在空气中燃烧的实验(如图),同学们观察到镁条在空气中剧烈燃烧,发出耀眼的强光,产生的大量白烟弥漫到空气中,最后在石棉网上得到一些白色固体. 
(1)请写出镁条燃烧的化学方程式;
(2)同学们通过称量发现:在石棉网上收集到产物的质量小于镁条的质量,有人认为这个反应不遵循质量守恒定律.你认为出现这样实验结果的原因可能是:
(3)小红按右下图装置改进实验,验证了质量守恒定律,还发现产物中有少量黄色固体. 
【提出问题】黄色固体是什么?
【查阅资料】①氧化镁为白色固体;②镁能与氮气剧烈反应产生黄色的氮化镁(Mg3N2)固体;③氮化镁可与水反应产生氨气,该气体能使湿润的红色石蕊试纸变蓝.
【做出猜想】黄色固体是Mg3N2
【实验探究】请设计实验,验证猜想
实验操作 | 实验现象及结论 |
(4)【反思与交流】①氮化镁中氮元素的化合价是; ②空气中N2的含量远大于O2的含量,可是镁条在空气中燃烧产物MgO却远多于Mg3N2 , 合理的解释是: .
③同学们又联想到氯气在氧气中能够燃烧,于是对燃烧条件又有了新的认识: .