题目内容
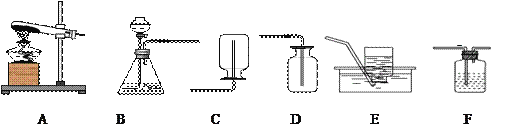
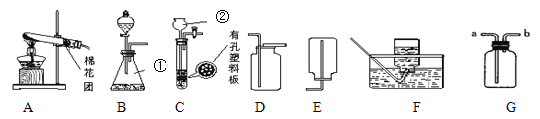
【题目】某校课外活动小组的同学在老师的帮助下,探究用赤铁矿(主要成分是 Fe2O3)炼铁的主要反应原理,他们设计的实验装置如图所示.
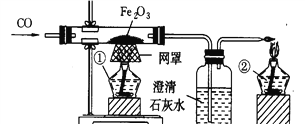

回答下列问题:
(1)写出用一氧化碳还原氧化铁的化学方程式________________________。
(2)实验时,在澄清石灰水中观察到的现象是______________________________。
(3)左图中设计第②个酒精灯的目的是____________________________,实验时应先点燃第_____个酒精灯。
(4)图(乙)与左图相比,它的主要优点是____________________。
【答案】 3CO+Fe2O3 ![]() 2Fe+3CO2 澄清石灰水变浑浊 防止一氧化碳污染空气 ② 节能
2Fe+3CO2 澄清石灰水变浑浊 防止一氧化碳污染空气 ② 节能
【解析】(1)一氧化碳与氧化铁在高温条件下反应生成铁和二氧化碳,反应的化学方程式为: ![]()
![]()
![]() ;(2)生成的二氧化碳能与澄清石灰水反应生成碳酸钙沉淀和水,故可以观察到澄清石灰水变浑浊,反应的化学方程式为:
;(2)生成的二氧化碳能与澄清石灰水反应生成碳酸钙沉淀和水,故可以观察到澄清石灰水变浑浊,反应的化学方程式为: ![]() ;(3)一氧化碳有毒,排放到空气中会污染空气,一氧化碳与氧气在点燃条件下反应生成二氧化碳,故设计第②个酒精灯可防止未反应的一氧化碳排放到空气中污染空气;因为要先通一氧化碳排净玻璃管内的空气,而一氧化碳有毒不能排放到空气中去,所以要先点燃第②个酒精灯;(4)图(乙)与左图相比,主要优点是利用了一氧化碳的可燃性,节约燃料,减少空气污染。
;(3)一氧化碳有毒,排放到空气中会污染空气,一氧化碳与氧气在点燃条件下反应生成二氧化碳,故设计第②个酒精灯可防止未反应的一氧化碳排放到空气中污染空气;因为要先通一氧化碳排净玻璃管内的空气,而一氧化碳有毒不能排放到空气中去,所以要先点燃第②个酒精灯;(4)图(乙)与左图相比,主要优点是利用了一氧化碳的可燃性,节约燃料,减少空气污染。

练习册系列答案
相关题目