题目内容
【题目】为了研究炼铁的主要反应原理,某化学兴趣小组的同学用一氧化碳还原氧化铁做实验。装置如下图所示。请回答下列问题:
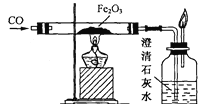
(1)在实验开始后可观察到如下现象:玻璃管中的粉末由_______色逐渐变为_______色,这说明了氧化铁在反应中失去了_______而被还原,这种粉末就是被还原出来的_______;澄清石灰水中出现_______,这说明一氧化碳夺取了氧化铁中的_______而被氧化,产生了_______气体。
(2)若一氧化碳是足量的,要制得56 g铁,至少需要氧化铁_______g,同时能产生二氧化碳_______g。
【答案】 红棕 黑 氧 铁粉 浑浊 氧 CO2 80 66
【解析】(1)氧化铁是红棕色固体,能与一氧化碳反应生成黑色的铁粉和气体二氧化碳,在实验开始后可观察到如下现象:玻璃管中的粉末由红棕色逐渐变为黑色,这说明了氧化铁在反应中失去了氧而被还原,这种粉末就是被还原出来的铁粉;二氧化碳能氢氧化钙反应生成碳酸钙沉淀和水,澄清石灰水中出现白色沉淀,这说明一氧化碳夺取了氧化铁中的氧而被氧化,产生了二氧化碳气体;(2)设要制得56 g铁,至少需要氧化铁的质量为x,同时能产生二氧化碳的质量为y。
Fe2O3+3CO ![]() 2Fe + 3CO2
2Fe + 3CO2
160 112 132
x 56g y
160/x=112/56g x=80g
112/56g=132/y y=66g
答:若一氧化碳是足量的,要制得56 g铁,至少需要氧化铁80g,同时能产生二氧化碳60g。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目