题目内容
【题目】如图所示是甲、乙两种固体物质的溶解度曲线,回答下列问题:
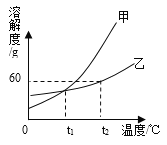
(1)p点的含义____________________________。
(2)若甲中含有少量的乙,则提纯甲可以采用的方法是___________。
(3)t2℃时,把50g乙物质放入50g水中,充分搅拌,所得溶液质量是_____g。
(4)t2℃时,配制等质量的甲乙两种饱和溶液需要水的质量:甲____乙(>;<;=)。
【答案】 t1℃甲乙两种物质的溶解度相等 降温结晶(或冷却热饱和溶液) 80 <
【解析】(1)由溶解度曲线可以:交点的含义是两物质的溶解度相等;
(2)根据物质的溶解度受温度的影响解答;
(3)根据溶液是否饱和解答;
(4)根据物质的溶解度解答。
解:(1)P点是曲线甲乙的交点,故其含义是:t1℃甲乙两种物质的溶解度相等;
(2)甲、乙两物质的溶解度都随温度的升高而增大,且甲受温度的影响变化较大。故甲中含有少量的乙,则提纯甲可以采用的方法是:降温结晶(或冷却热饱和溶液);
(3)t2℃时,乙物质的溶解度为60g。即100g水中最多溶解60g乙物质,那么50g水中最多溶解30g乙物质。故t2℃时,把50g乙物质放入50g水中,充分搅拌,所得溶液质量是80g;
(4)t2℃时,甲物质的溶解度大于乙物质的溶解度。故t2℃时,配制等质量的甲乙两种饱和溶液需要水的质量:甲<乙。

 阅读快车系列答案
阅读快车系列答案【题目】某化学兴趣小组的同学在做氢氧化钙与盐酸中和反应的实验时,忘记滴加指示剂,因而无法判断酸碱是否恰好完全反应。于是他们对反应后溶液中的溶质大胆提出猜想,进行了以下探究,请你和他们一起完成下列实验报告。
Ⅰ.定性探究
【提出问题】该溶液中的溶质含有哪些成分?
【查阅资料】CaCl2溶液呈中性。
【猜想与假设】
猜想Ⅰ:溶液中的溶质只有____________;
猜想Ⅱ:溶液中的溶质有CaCl2、HCl;
猜想Ⅲ:溶液中的溶质有CaCl2、Ca(OH)2;
猜想Ⅳ:溶液中的溶质有CaCl2、Ca(OH)2、HCl。
(1)经过讨论,同学们直接得出不合理的猜想是哪一种并说出理由:___________________。
为了验证余下的哪一种猜想是正确的,同学们又做了以下实验。
【进行实验】研究
(2)
实验操作 | 实验现象 | 实验结论 |
①取少量反应后的溶液于试管中,滴加酚酞溶液 | 溶液不变色 | 猜想Ⅲ不正确 |
②再另取少量反应后的溶液于另一支试管中,向里面加入适量碳酸钠 | 有气泡产生 | 猜想_______正确 |
(3)操作②有气泡生成的化学方程式为_________________________。
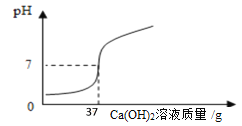
(4)下列曲线能够表示所做实验中溶液pH变化趋势的是________(填序号)。
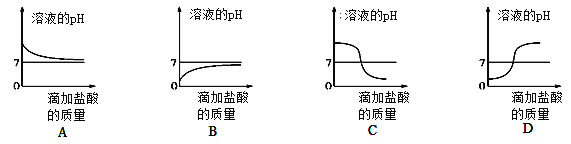
【反思交流】
(5)要使烧杯内溶液的溶质只含CaCl2,需要除去杂质,其中的一种方法是向烧杯中加入过量的_______________,然后过滤。
Ⅱ.定量探究
(6)兴趣小组同学想对本地化工厂排放废水中的HCl含量进行了测定(不含其他酸性物质)。取废水5 g,用质量分数为2%的氢氧化钙溶液进行中和,如下图所示。请你计算废水中HCl的质量分数。(写出具体的计算过程)___________