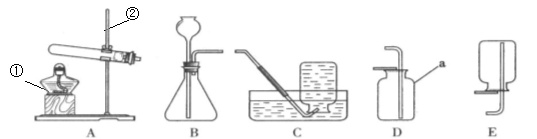��Ŀ����
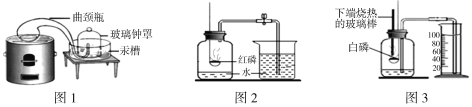
����Ŀ����������װ�ã��ش����⣺
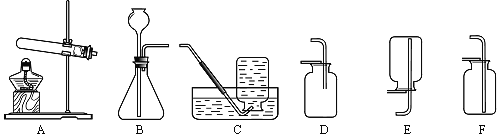
��1��ʵ������KMnO4��ȡO2����Ӧ�ķ��ű���ʽΪ ������װ��ѡ ������Cװ���ռ�O2����ʱ�䱣�棬������ ��
��2��ʵ�������ijС��ͬѧ������Ͷ��ˮ���У�������ҺΪī��ɫ��ҡ��ˮ�ۣ��ֱ���Ϻ�ɫ�������������� ������ѧʽ����Ե�ʡ�
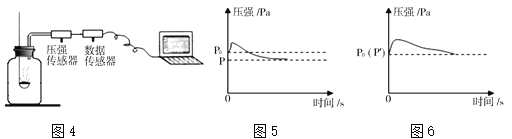
��3��Ϊ��һ���о�KMnO4����ʱ��ʧ���ʣ�ijС��������������ϣ��ش�
�����Ͽ�Ƭ����
1����Ӧ�й���ʧ����ΪO2��KMnO4�����ȣ�
2���о�������KMnO4���ȷֽ�ʱ����Ҫ��������������Ӧ��
a��KMnO4![]() K2MnO4+K2Mn4O8+O2����ʧ����ԼΪ13.5����
K2MnO4+K2Mn4O8+O2����ʧ����ԼΪ13.5����
B��KMnO4![]() KMnO2+O2����ʧ����ԼΪ20.3����
KMnO2+O2����ʧ����ԼΪ20.3����
��ȡ8.0gKMnO4������ʹ֮��ȫ�ֽ⣬����O2����������Ϊ
A��0.81g B��1.08g C��1.42g D��1.63g
����43.9��~377.9����Χ�У�KMnO4��ʧ����Ϊ18.0%��������Ϸ�������43.9��~377.9����Χ�У�KMnO4�ֽⷴӦ��Ҫ�� ���a����B����Ϊ����
���𰸡���1��KMnO4��KMnO4+K2MnO4+O2��A���ռ�ʱ������ƿ�ײ�����ˮ����������ƿ������ʵ��̨�ϡ���2��KMnO4����3����C����B
��������
���������ʵ������KMnO4��ȡO2����Ӧ�ķ��ű���ʽΪKMnO4 �� KMnO4 + K2MnO4 + O2������װ��ѡA����������Ҫ���ȣ�����Cװ���ռ�O2����ʱ�䱣�棬�������ռ�ʱ������ƿ�ײ�����ˮ����������ƿ������ʵ��̨�ϡ�ʵ�������ijС��ͬѧ������Ͷ��ˮ���У�������ҺΪī��ɫ��ҡ��ˮ�ۣ��ֱ���Ϻ�ɫ��������������KMnO4��Ե�ʣ�ȡ8.0gKMnO4������ʹ֮��ȫ�ֽ⣬����O2����������Ϊ8��*13.5%=1.08�ˣ�������8��*20.3%=1.63�ˣ����Բ��������������������Χ������43.9��~377.9����Χ�У�KMnO4��ʧ����Ϊ18.0%��������Ϸ�������43.9��~377.9����Χ�У�KMnO4�ֽⷴӦ��Ҫ��BΪ������ΪB��Ӧ����ʧ�ر���20.3%��

 ��ѧʵ����ϵ�д�
��ѧʵ����ϵ�д�