题目内容
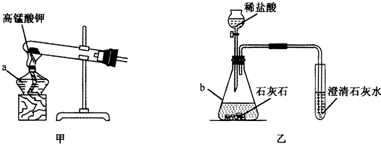
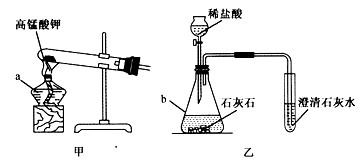
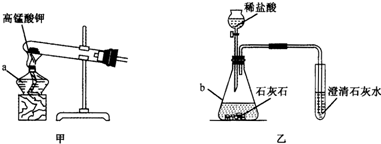
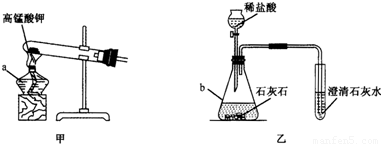
观察下列装置图,回答有关问题:
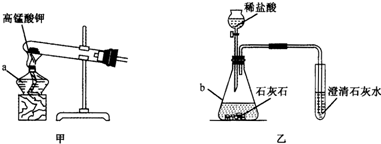
(1)写出有标号仪器的名称:a______,b______.
(2)实验室用甲装置制氧气的化学方程式为______.反应结束后冷却,往试管中加入足量的水,搅拌、过滤,得到黑色粉末.该黑色粉末与过氧化氢接触有大量气泡产生,黑色粉末在反应中的作用是______.
(3)某化学兴趣小组用乙装置制取并检验二氧化碳.实验过程中,可观察到试管里产生白色沉淀,该反应的化学方程式是______.
(4)产生沉淀后继续通入二氧化碳,过一段时间后,发现沉淀溶解变成澄清溶液.通过 探究得知,生成的沉淀能够与二氧化碳、水发生化合反应生成可溶于水的碳酸氢钙,则反应的化学方程式为:______.
(5)由二氧化碳通入澄清的石灰水所产生的不同现象,你得到的启示是______.
解:(1)根据常用仪器可知仪器分别是:酒精灯和锥形瓶;
(2)高锰酸钾在加热的条件下生成锰酸钾、二氧化锰和氧气,方程式是2KMnO4 K2MnO4+MnO2+O2↑,根据题中信息可知,该黑色粉末能改变过氧化氢的化学反应速率,可知是高锰酸钾分解后的二氧化锰,它不溶于水,在过氧化氢反应中起催化作用;
K2MnO4+MnO2+O2↑,根据题中信息可知,该黑色粉末能改变过氧化氢的化学反应速率,可知是高锰酸钾分解后的二氧化锰,它不溶于水,在过氧化氢反应中起催化作用;
(3)二氧化碳与石灰水的主要成分氢氧化钙反应生成碳酸钙沉淀和水,方程式是CO2+Ca(OH)2=CaCO3↓+H2O;
(4)根据题意,碳酸钙与二氧化碳、水发生化合反应生成可溶于水的碳酸氢钙,方程式是CaCO3+H2O+CO2=Ca(HCO3)2;
(5)根据实验现象,我们可以得到许多启示:反应物的量不同,实验现象不同;反应物的量不同,反应产物不同;对某
些化学反应,应控制反应物的量等(答案合理即可).
故答案为:
(1)酒精灯 锥形瓶
(2)2KMnO K2MnO4+MnO2+O2↑ 催化作用
K2MnO4+MnO2+O2↑ 催化作用
(3)CO2+Ca(OH)2=CaCO3↓+H2O
(4)CaCO3+H2O+CO2=Ca(HCO3)2
(5)反应物的量不同,实验现象不同;反应物的量不同,反应产物不同;对某
些化学反应,应控制反应物的量等(答案合理即可).
分析:(1)根据常用仪器的名称和用途解答;
(2)根据高锰酸钾分解的反应原理书写方程式,根据信息可知,该黑色粉末能改变过氧化氢的化学反应速率,可知是高锰酸钾分解后的二氧化锰,它不溶于水,在过氧化氢反应中起催化作用;
(3)根据二氧化碳与石灰水的反应原理书写方程式;
(4)根据反应物、生成物书写方程式;
(5)针对题目要求和实验现象,经过合理分析、推导后回答.
点评:本题涉及实验室制取氧气的反应原理及对催化剂的考查,并考查了同学们根据题意提供的信息分析问题的能力,同学们在平时除了要学好基础知识外,还要多实验,勤思考.
(2)高锰酸钾在加热的条件下生成锰酸钾、二氧化锰和氧气,方程式是2KMnO4
 K2MnO4+MnO2+O2↑,根据题中信息可知,该黑色粉末能改变过氧化氢的化学反应速率,可知是高锰酸钾分解后的二氧化锰,它不溶于水,在过氧化氢反应中起催化作用;
K2MnO4+MnO2+O2↑,根据题中信息可知,该黑色粉末能改变过氧化氢的化学反应速率,可知是高锰酸钾分解后的二氧化锰,它不溶于水,在过氧化氢反应中起催化作用;(3)二氧化碳与石灰水的主要成分氢氧化钙反应生成碳酸钙沉淀和水,方程式是CO2+Ca(OH)2=CaCO3↓+H2O;
(4)根据题意,碳酸钙与二氧化碳、水发生化合反应生成可溶于水的碳酸氢钙,方程式是CaCO3+H2O+CO2=Ca(HCO3)2;
(5)根据实验现象,我们可以得到许多启示:反应物的量不同,实验现象不同;反应物的量不同,反应产物不同;对某
些化学反应,应控制反应物的量等(答案合理即可).
故答案为:
(1)酒精灯 锥形瓶
(2)2KMnO
 K2MnO4+MnO2+O2↑ 催化作用
K2MnO4+MnO2+O2↑ 催化作用(3)CO2+Ca(OH)2=CaCO3↓+H2O
(4)CaCO3+H2O+CO2=Ca(HCO3)2
(5)反应物的量不同,实验现象不同;反应物的量不同,反应产物不同;对某
些化学反应,应控制反应物的量等(答案合理即可).
分析:(1)根据常用仪器的名称和用途解答;
(2)根据高锰酸钾分解的反应原理书写方程式,根据信息可知,该黑色粉末能改变过氧化氢的化学反应速率,可知是高锰酸钾分解后的二氧化锰,它不溶于水,在过氧化氢反应中起催化作用;
(3)根据二氧化碳与石灰水的反应原理书写方程式;
(4)根据反应物、生成物书写方程式;
(5)针对题目要求和实验现象,经过合理分析、推导后回答.
点评:本题涉及实验室制取氧气的反应原理及对催化剂的考查,并考查了同学们根据题意提供的信息分析问题的能力,同学们在平时除了要学好基础知识外,还要多实验,勤思考.

练习册系列答案
相关题目