题目内容
【题目】如图是某同学配制溶液的过程:
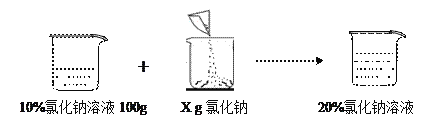
根据图中数据,求:
(1)原溶液中的溶质质量为 g ,溶剂质量为 g。
(2)若通过蒸发水的方法使其变为20%的溶液,蒸发水的质量为 g。
(3)求上图中加入氯化钠的质量X?
【答案】(1)10;90;(2)50;(3)12.5g
【解析】加入溶质可以使得稀溶液的浓度变大,则在此过程中稀溶液中溶质的质量+溶解的溶质=浓溶液中溶质的溶质;蒸发溶剂也可以使得稀溶液变成浓溶液,在此过程中稀溶液中溶质的质量=浓溶液中溶质的质量-析出溶质质量。(1)原溶液中氯化钠的质量为10%![]() 100g,溶剂为100g-10%
100g,溶剂为100g-10%![]() 100g=90g,加入Xg溶质后变成了20%的溶液,此时溶液中溶质的质量为20%
100g=90g,加入Xg溶质后变成了20%的溶液,此时溶液中溶质的质量为20%![]() (100+x)g,故10%
(100+x)g,故10%![]() 100g+x=20%
100g+x=20%![]() (100+x)g,X=10g;(2)蒸发水的使得溶液浓度变为20%,此过程中溶质的质量未变化,故可以根据蒸发前溶液中溶质质量=蒸发后溶液中溶质的质量可得10%
(100+x)g,X=10g;(2)蒸发水的使得溶液浓度变为20%,此过程中溶质的质量未变化,故可以根据蒸发前溶液中溶质质量=蒸发后溶液中溶质的质量可得10%![]() 100g =20%
100g =20%![]() (100-x)g,X=50g;(3)原溶液中氯化钠的质量为10%
(100-x)g,X=50g;(3)原溶液中氯化钠的质量为10%![]() 100g加入Xg溶质后变成了20%的溶液,此时溶液中溶质的质量为20%
100g加入Xg溶质后变成了20%的溶液,此时溶液中溶质的质量为20%![]() (100+x)g,故10%
(100+x)g,故10%![]() 100g+x=20%
100g+x=20%![]() (100+x)g,X=12.5g。
(100+x)g,X=12.5g。

【题目】某化学兴趣小组的同学采用了下图所示装置测定空气中氧气含量。
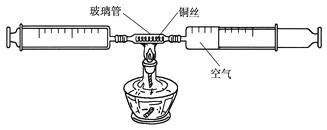
在由两个注射器组成的密闭系统中留有25mL空气,给装有细铜丝的玻璃管加热,同时缓慢推动两个注射器活塞,至玻璃管内的铜丝在较长时间内无进一步变化时停止加热,待冷却至室温,将气体全部推至一个注射器内,观察密闭系统内空气体积变化。
(1)在实验加热过程中,交替缓慢推动两个注射器活塞的目的是__________________;
(2)写出该实验过程中玻璃管内的现象为_______________________________,写出该反应的符号表达式________________________________;
(3)小强实验操作均正确,测得实验结果如下:
反应前注射器内气体总体积 | 反应后注射器内气体总体积 |
25mL | 20mL |
该实验得出的结论为 ____________________________________;
小红同学实验误差较大,请你帮她分析造成误差的原因_____________(写出一条即可)。