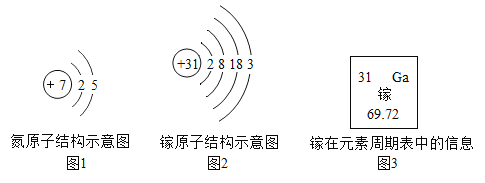
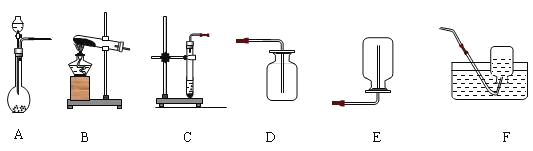
题目内容
【题目】某中学的一个化学兴趣小组用石灰石和盐酸制取一瓶CO2,验满后,将澄清石灰水倒入集气瓶中,发现没有变浑浊。兴趣小组对这个异常现象进行了探究。
[提出问题]澄清石灰水为什么没有变浑浊?
[查阅资料] (1)CO2过量时,CaCO3沉淀会转化为可溶于水的Ca(HCO3)2
(2)AgCl不溶于稀硝酸
[提出猜想]Ⅰ、石灰水已完全变质Ⅱ、_____Ⅲ。 CO2 中混有HCl
[实验方案]兴趣小组用原药品继续制取CO2,并进行探究。制备CO2的化学方程式为_____。
步骤 | 实验操作 | 实验现象 | 结论及化学方程式 |
(1) | 取少量澄清石灰水于试管中,加入碳酸钠溶液。 | 产生白色沉淀。 | 猜想I不成立。 |
(2) | 将少量气体通入盛有澄清石灰水的试管中。 | _____ | 猜想Ⅱ不成立。 |
(3) | 将气体通入盛有硝酸银溶液的试管中,再加稀硝酸。 | 产生白色沉淀 | 猜想Ⅲ成立。反应方程式为 _____ |
[实验结论]制取的CO2气体中混入了HCl,所以澄清石灰水没有变浑浊。
[交流讨论]若要收集到纯净、干燥的CO2,需将混合气体依次通入饱和NaHCO3溶液和_____。
[拓展思考]回忆课本中收集呼出气体的操作后,同学们尝试用排水法收集一瓶CO2,倒入澄清石灰水后,石灰水变浑浊。你认为该实验成功的原因是_____(写一点)。
【答案】二氧化碳过量 ![]() 不产生白色沉淀
不产生白色沉淀 ![]() 浓硫酸 氯化氢溶于水
浓硫酸 氯化氢溶于水
【解析】
碳酸钙和稀盐酸反应生成氯化钙、水和二氧化碳,二氧化碳和氢氧化钙反应生成碳酸钙和水,硝酸银和盐酸反应生成氯化银和硝酸。
[提出猜想] CO2过量时,CaCO3沉淀会转化为可溶于水的Ca(HCO3)2,故Ⅱ、二氧化碳过量。
[实验方案]碳酸钙和稀盐酸反应生成氯化钙、水和二氧化碳,故制备CO2的化学方程式为![]() 。
。
氢氧化钙和碳酸钠反应生成碳酸钙和氢氧化钠,二氧化碳和氢氧化钙反应生成碳酸钙和水,由于少量二氧化碳也不能使石灰水变浑浊所以不是二氧化碳过量的原因,硝酸银和盐酸反应生成氯化银和硝酸。
步骤 | 实验操作 | 实验现象 | 结论及化学方程式 |
(1) | 取少量澄清石灰水于试管中,加入碳酸钠溶液。 | 产生白色沉淀。 | 猜想I不成立。 |
(2) | 将少量气体通入盛有澄清石灰水的试管中。 | 不产生白色沉淀 | 猜想Ⅱ不成立。 |
(3) | 将气体通入盛有硝酸银溶液的试管中,再加稀硝酸。 | 产生白色沉淀 | 猜想Ⅲ成立。反应方程式为 |
[交流讨论]盐酸和碳酸氢钠反应生成碳酸钠和水和二氧化碳,浓硫酸具有吸水性,可以吸收水分,故若要收集到纯净、干燥的CO2,需将混合气体依次通入饱和NaHCO3溶液和浓硫酸进行除杂和干燥。
[拓展思考] 氯化氢溶于水,通过水除去了氯化氢,故用排水法收集一瓶CO2,倒入澄清石灰水后,石灰水变浑浊,该实验成功的原因是氯化氢溶于水。